| نترات الأمونيوم سيريك: نترات الأمونيوم سيريك (CAN) هو مركب غير عضوي بالصيغة ( NH 4 ) 2 Ce (NO 3 ) 6 . ملح السيريوم البرتقالي والأحمر القابل للذوبان في الماء هو عامل مؤكسد متخصص في التركيب العضوي ومؤكسد قياسي في التحليل الكمي |  |
| كلورات الأمونيوم: كلورات الأمونيوم مركب غير عضوي مع الصيغة NH 4 ClO 3 . |  |
| كلوريد الأمونيوم: كلوريد الأمونيوم مركب غير عضوي مع الصيغة NH 4 Cl وملح بلوري أبيض قابل للذوبان في الماء بدرجة عالية. محاليل كلوريد الأمونيوم حمضية بشكل معتدل. Sal ammoniac هو اسم للشكل الطبيعي والمعدني لكلوريد الأمونيوم. يتكون المعدن بشكل شائع عند حرق مقالب الفحم من تكثيف الغازات المشتقة من الفحم. يوجد أيضًا حول بعض أنواع الفتحات البركانية. يستخدم بشكل أساسي كسماد وعامل توابل في بعض أنواع عرق السوس. إنه ناتج عن تفاعل حمض الهيدروكلوريك والأمونيا. |  |
| سداسي كلورو بلاتينات الأمونيوم: سداسي كلورو بلاتينات الأمونيوم ، المعروف أيضًا باسم كلوروبلاتينات الأمونيوم ، هو مركب غير عضوي له الصيغة (NH 4 ) 2 [PtCl 6 ]. إنه مثال نادر لملح البلاتين (IV) القابل للذوبان غير المرطب. يشكل محاليل صفراء مكثفة في الماء. في وجود 1M NH 4 Cl ، تكون قابليته للذوبان 0.0028 جم / 100 مل. |  |
| كرومات الأمونيوم: الأمونيوم كرومات هو الملح مع الصيغة (NH 4) 2 كرو 4. تشكل بلورات صفراء أحادية الميل. مصنوعة من هيدروكسيد الأمونيوم وثاني كرومات الأمونيوم ؛ يستخدم في التصوير الفوتوغرافي كمحفز لطلاء الجيلاتين. غالبًا ما يستخدم في التصوير الفوتوغرافي وطباعة المنسوجات وتثبيت صبغات الكرومات على الصوف. كما أنه يستخدم ككاشف تحليلي ومحفز ومانع للتآكل. وهو قابل للذوبان في الماء ، وعند استخدامه ، يمكن أن يسبب تهيجًا في الغشاء المخاطي والعينين والجهاز التنفسي والجلد ، وما إلى ذلك. وقد يسبب حساسية للجلد بعد ملامسته لفترة طويلة. ومن المعروف أيضًا أنها مادة مسرطنة (مسببة للسرطان) ، ويمكن أن تسبب تقرح الأنسجة وإصابة الكبد والكلى. |  |
| الشب: الشب هو نوع من المركبات الكيميائية ، وعادة ما يكون ملح كبريتات مزدوج مائي من الألومنيوم مع الصيغة العامة X Al (SO |  |
| سيانات الأمونيوم: سيانات الأمونيوم مركب غير عضوي بالصيغة NH 4 OCN. إنها مادة صلبة عديمة اللون. |  |
| سيانيد الأمونيوم: سيانيد الأمونيوم مركب غير عضوي غير مستقر بالصيغة NH 4 CN. | 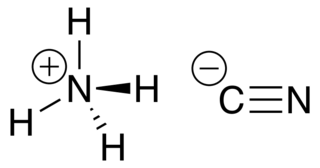 |
| ثاني كرومات الأمونيوم: ثنائي كرومات الأمونيوم مركب غير عضوي بالصيغة (NH 4 ) 2 Cr 2 O 7 . في هذا المركب ، كما هو الحال في جميع الكرومات وثنائي كرومات ، يكون الكروم في حالة أكسدة +6 ، والمعروف باسم الكروم سداسي التكافؤ. وهو ملح يتكون من أيونات الأمونيوم وأيونات ثنائي كرومات. |  |
| الأمونيوم ثنائي إيثيل ثنائي الفوسفات: الأمونيوم ثنائي إيثيل ثنائي الفوسفات أو الأمونيوم بشكل أكثر منهجية O ، O ′ -diethyl dithiophosphate ، هو ملح الأمونيوم لحمض ثنائي إيثيل ديثيوفوسفوريك. يتم استخدامه كمصدر لـ (C 2 H 5 O) 2 PS 2 - يجند في كيمياء التنسيق وفي الكيمياء التحليلية لتحديد الأيونات المختلفة. يمكن الحصول عليها عن طريق تفاعل الفوسفور بنتاسولفيد مع الإيثانول والأمونيا. في التركيب البلوري لهذا المركب ، يتم توصيل كاتيون الأمونيوم بأربعة روابط هيدروجينية N-H ··· S مدعومة بالشحن إلى أربعة أنيونات ثنائي إيثيل ثنائي الفوسفات رباعي السطوح. |  |
| فوسفات هيدروجين الأمونيوم: فوسفات هيدروجين الأمونيوم ( ADP ) ، المعروف أيضًا باسم فوسفات الأمونيوم الأحادي ( MAP ) هو مركب كيميائي له الصيغة الكيميائية (NH 4 ) (H 2 PO 4 ). ADP هو عنصر رئيسي في الأسمدة الزراعية وبعض طفايات الحريق. كما أن لها استخدامات كبيرة في البصريات والإلكترونيات. |  |
| فوسفات هيدروجين الأمونيوم: فوسفات هيدروجين الأمونيوم ( ADP ) ، المعروف أيضًا باسم فوسفات الأمونيوم الأحادي ( MAP ) هو مركب كيميائي له الصيغة الكيميائية (NH 4 ) (H 2 PO 4 ). ADP هو عنصر رئيسي في الأسمدة الزراعية وبعض طفايات الحريق. كما أن لها استخدامات كبيرة في البصريات والإلكترونيات. |  |
| ثنائي موليبدات الأمونيوم: ثنائي موليبدات الأمونيوم (ADM) هو مركب غير عضوي بالصيغة (NH 4 ) 2 Mo 2 O 7 . وهي مادة صلبة بيضاء قابلة للذوبان في الماء. ADM هو وسيط في إنتاج مركبات الموليبدينوم من خاماته. ينتج عن تحميص الخام النموذجي أكاسيد الموليبدينوم الخام (VI) ، والتي يمكن استخلاصها إلى أمونيا مائية ، مما يوفر موليبدات الأمونيوم. تعطي حلول تسخين موليبدات الأمونيوم ADM. عند التسخين ، يتحلل ثنائي ديوليبدات الأمونيوم الصلب إلى ثالث أكسيد الموليبدينوم:
| |
| ثنائي نترات الأمونيوم: ثنائي نترات الأمونيوم ( ADN ) هو ملح الأمونيوم لحمض الدينيترامينيك. يتحلل ADN تحت الحرارة ليترك فقط النيتروجين والأكسجين والماء. الأيونات هي أيون الأمونيوم NH 4 + و ثنائي نتراميد N (NO 2 ) 2 - . |  |
| ديورانات الأمونيوم: ديورانات الأمونيوم أو (ADU) ((NH 4 ) 2 U 2 O 7 ) ، هو أحد الأشكال الكيميائية الوسيطة المشعة لليورانيوم المنتج أثناء إنتاج الكعكة الصفراء. الاسم "الكعكة الصفراء" الذي أطلق في الأصل على هذا الملح الأصفر اللامع ، ينطبق الآن على خليط من أكاسيد اليورانيوم التي بالكاد صفراء. كما أنه وسيط في تصنيع الوقود بأكسيد مختلط (MOX). على الرغم من أنه يطلق عليه عادة "ديورانات الأمونيوم" كما لو أنه يحتوي على "ديورانات" أيون يو |  |
| كبريتات الأمونيوم لوريل: كبريتات لوريل الأمونيوم (ALS) هو الاسم الشائع لكبريتات الأمونيوم دوديسيل (CH 3 (CH 2 ) 10 CH 2 OSO 3 NH 4 ). يتكون الأنيون من سلسلة هيدروكربونية غير قطبية ومجموعة نهائية قطبية للكبريتات. يمنح الجمع بين المجموعات غير القطبية والمجموعات القطبية خصائص الفاعل بالسطح للأنيون: فهو يسهل انحلال كل من المواد القطبية وغير القطبية. يصنف ALS على أنه إستر كبريتات. يوجد بشكل أساسي في الشامبو وغسول الجسم كعامل رغوة. / كبريتات لوريل هي مواد خافضة للتوتر السطحي عالية الرغوة تعطل التوتر السطحي للماء جزئيًا عن طريق تكوين المذيلات في واجهة الهواء السطحي. | |
| سترات الأمونيوم الحديديك: سيترات الأمونيوم الحديديك لها الصيغة (NH 4 ) 5 [Fe (C 6 H 4 O 7 ) 2 ]. السمة المميزة لهذا المركب هي أنه قابل للذوبان في الماء بشكل كبير ، على عكس سترات الحديديك غير القابلة للذوبان بشكل كبير. |  |
| أكسالات الأمونيوم الحديديك: أكسالات الأمونيوم الحديديك هو ملح الأمونيوم لمركب تنسيق تريسوكسالاتو الأنيوني للحديد (III). إنه مقدمة لأكاسيد الحديد ، والبوليمرات التنسيقية المتنوعة ، والأزرق البروسي. يرتبط السلوك الأخير بتصنيع ورق المخطط. |  |
| فلوريد الأمونيوم: فلوريد الأمونيوم هو مركب غير عضوي مع الصيغة NH 4 F. وهو يتبلور على شكل موشورات صغيرة عديمة اللون ، وله طعم ملحي حاد ، وقابل للذوبان في الماء بدرجة عالية. مثل جميع أملاح الفلوريد ، فهو معتدل السمية في كل من الجرعة الزائدة الحادة والمزمنة. |  |
| الأمونيوم فلوروسيليكات: فلوروسيليكات الأمونيوم (المعروف أيضًا باسم سداسي فلوروسيليكات الأمونيوم أو فلوسيليكات الأمونيوم أو سيليكوفلوريد الأمونيوم) له الصيغة (NH 4 ) 2 SiF 6 . إنها مادة كيميائية سامة ، مثل جميع أملاح حمض الفلوروسيليك. وهي مصنوعة من بلورات بيضاء ، والتي لها ما لا يقل عن ثلاثة أشكال متعددة وتظهر في الطبيعة كمعادن نادرة كريبتوهاليت أو باراريت. |  |
| الأمونيوم فلوروسيليكات: فلوروسيليكات الأمونيوم (المعروف أيضًا باسم سداسي فلوروسيليكات الأمونيوم أو فلوسيليكات الأمونيوم أو سيليكوفلوريد الأمونيوم) له الصيغة (NH 4 ) 2 SiF 6 . إنها مادة كيميائية سامة ، مثل جميع أملاح حمض الفلوروسيليك. وهي مصنوعة من بلورات بيضاء ، والتي لها ما لا يقل عن ثلاثة أشكال متعددة وتظهر في الطبيعة كمعادن نادرة كريبتوهاليت أو باراريت. |  |
| الأمونيوم فورمات: فورمات الأمونيوم NH 4 HCO 2 هو ملح الأمونيوم لحمض الفورميك. وهو مادة صلبة بلورية عديمة اللون ومرطبة. | 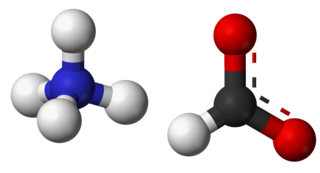 |
| فومارات الأمونيوم: فومارات الأمونيوم مركب له الصيغة (NH 4 ) 2 (C 2 H 2 (COO) 2 ). إنه ملح الأمونيوم لحمض الفوماريك. كمادة مضافة للغذاء ، لديها رقم E E368. |  |
| جلوتامات أحادي الأمونيوم: غلوتامات أحادي الأمونيوم مركب له الصيغة NH 4 C 5 H 8 NO 4 . إنه ملح حمض الأمونيوم لحمض الجلوتاميك. |  |
| الأمونيوم: كاتيون الأمونيوم هو أيون متعدد الذرات موجب الشحنة مع الصيغة الكيميائية NH + | 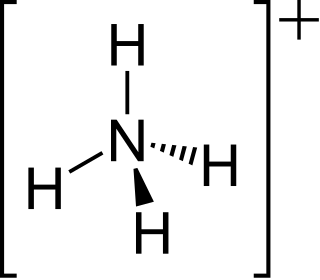 |
| الأمونيوم هيبتاموليبدات: الأمونيوم heptamolybdate هو مركب غير العضوية التي الصيغة الكيميائية هي (NH 4) 6 مو 7 O 24، واجه عادة باسم tetrahydrate. ثنائي الهيدرات معروف أيضًا. وهي مادة صلبة عديمة اللون ، يشار إليها غالبًا باسم باراموليبدات الأمونيوم أو ببساطة موليبدات الأمونيوم ، على الرغم من أن "موليبدات الأمونيوم" يمكن أن يشير أيضًا إلى أورثوموليبدات الأمونيوم ، (NH 4 ) 2 MoO 4 ، والعديد من المركبات الأخرى. إنه أحد أكثر مركبات الموليبدينوم شيوعًا. |  |
| سداسي كلوروريدات الأمونيوم (IV): سداسي كلوروريدات الأمونيوم (IV) هو مركب غير عضوي له الصيغة (NH 4 ) 2 [IrCl 6 ]. هذه المادة الصلبة ذات اللون البني الداكن هي ملح الأمونيوم لمركب الإريديوم (IV) [IrCl 6 ] 2− . إنه مركب إيريديوم مهم تجاريًا وهو أحد أكثر مجمعات الإيريديوم شيوعًا (IV). مركب مرتبط ولكن غير واضح هو الإيريديوم رباعي كلوريد ، والذي غالبًا ما يستخدم بالتبادل. |  |
| سداسي كلوروريدات الأمونيوم (IV): سداسي كلوروريدات الأمونيوم (IV) هو مركب غير عضوي له الصيغة (NH 4 ) 2 [IrCl 6 ]. هذه المادة الصلبة ذات اللون البني الداكن هي ملح الأمونيوم لمركب الإريديوم (IV) [IrCl 6 ] 2− . إنه مركب إيريديوم مهم تجاريًا وهو أحد أكثر مجمعات الإيريديوم شيوعًا (IV). مركب مرتبط ولكن غير واضح هو الإيريديوم رباعي كلوريد ، والذي غالبًا ما يستخدم بالتبادل. |  |
| سداسي كلورو بلاتينات الأمونيوم: سداسي كلورو بلاتينات الأمونيوم ، المعروف أيضًا باسم كلوروبلاتينات الأمونيوم ، هو مركب غير عضوي له الصيغة (NH 4 ) 2 [PtCl 6 ]. إنه مثال نادر لملح البلاتين (IV) القابل للذوبان غير المرطب. يشكل محاليل صفراء مكثفة في الماء. في وجود 1M NH 4 Cl ، تكون قابليته للذوبان 0.0028 جم / 100 مل. |  |
| سداسي فلورو ألومينات الأمونيوم: الأمونيوم hexafluoroaluminate هو مركب غير عضوي له الصيغة الكيميائية (NH 4) 3 [مؤسسة آنا ليند 6]. إنها مادة صلبة بيضاء. عند التسخين ، يتحول إلى ثلاثي فلوريد الألومنيوم ، وهو تفاعل يطلق فلوريد الهيدروجين. كما تم استخدامه كمقدمة للزيوليت. |  |
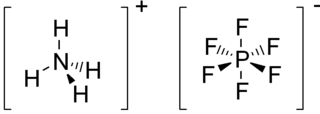
| سداسي فلورو فوسفات الأمونيوم: سداسي فلورو فوسفات الأمونيوم هو مركب غير عضوي بالصيغة NH 4 PF 6 . وهو مادة صلبة قابلة للذوبان في الماء ، واسترطابية. المركب عبارة عن ملح يتكون من كاتيون الأمونيوم وأنيون سداسي فلورو الفوسفات. يشيع استخدامه كمصدر لأنيون سداسي فلورو الفوسفات ، وهو أنيون ضعيف التنسيق. يتم تحضيره عن طريق الجمع بين فلوريد الأمونيوم الأنيق وخماسي كلوريد الفوسفور. بدلاً من ذلك ، يمكن أيضًا إنتاجه من كلوريد الفوسفونتريليك:
|  |
| الأمونيوم فلوروسيليكات: فلوروسيليكات الأمونيوم (المعروف أيضًا باسم سداسي فلوروسيليكات الأمونيوم أو فلوسيليكات الأمونيوم أو سيليكوفلوريد الأمونيوم) له الصيغة (NH 4 ) 2 SiF 6 . إنها مادة كيميائية سامة ، مثل جميع أملاح حمض الفلوروسيليك. وهي مصنوعة من بلورات بيضاء ، والتي لها ما لا يقل عن ثلاثة أشكال متعددة وتظهر في الطبيعة كمعادن نادرة كريبتوهاليت أو باراريت. |  |
| محلول الأمونيا: محلول الأمونيا، المعروف أيضا باسم المياه الأمونيا، وهيدروكسيد الأمونيوم، الخمور نشادرية، الخمور الأمونيا، ماء النشادر، والأمونيا مائي، أو (غير دقيق) الأمونيا، هو حل من الأمونيا في الماء. يمكن الإشارة إليه بالرموز NH 3 (aq). على الرغم من أن هيدروكسيد الأمونيوم اسم يدل على وجود القلويات مع تكوين [NH 4 +] [OH -]، فإنه من المستحيل فعليا لعينات عزل من NH 4 OH. الأيونات NH 4 + وOH - لا تمثل جزءا كبيرا من المبلغ الإجمالي من الأمونيا إلا في الحلول المخففة للغاية. | |
| ثنائي فلوريد الأمونيوم: فلوريد هيدروجين الأمونيوم هو مركب غير عضوي بالصيغة NH 4 HF 2 أو NH 4 F · HF. يتم إنتاجه من الأمونيا وفلوريد الهيدروجين. هذا الملح عديم اللون هو خدعة زجاجية وسيط في طريق تم التفكير فيه مرة واحدة لحمض الهيدروفلوريك. |  |
| بيكربونات الأمونيوم: بيكربونات الأمونيوم هو مركب غير عضوي مع صيغة (NH 4) HCO 3، مبسطة لNH 5 CO 3. المجمع له أسماء عديدة تعكس تاريخه الطويل. من الناحية الكيميائية ، هو ملح بيكربونات أيون الأمونيوم. إنه مادة صلبة عديمة اللون تتحلل بسهولة إلى ثاني أكسيد الكربون والماء والأمونيا. |  |
| ثنائي فلوريد الأمونيوم: فلوريد هيدروجين الأمونيوم هو مركب غير عضوي بالصيغة NH 4 HF 2 أو NH 4 F · HF. يتم إنتاجه من الأمونيا وفلوريد الهيدروجين. هذا الملح عديم اللون هو خدعة زجاجية وسيط في طريق تم التفكير فيه مرة واحدة لحمض الهيدروفلوريك. |  |
| ثنائي كبريتات الأمونيوم: ثنائي كبريتات الأمونيوم ، المعروف أيضًا باسم كبريتات هيدروجين الأمونيوم ، هو مادة صلبة بلورية بيضاء مع الصيغة (NH 4 ) HSO 4 . هذا الملح هو نتاج نصف معادلة لحمض الكبريتيك بواسطة الأمونيا. |  |
| هيدرو كبريتيد الأمونيوم: هيدرو كبريتيد الأمونيوم هو مركب كيميائي له الصيغة (NH 4 ) HS. |  |
| ثنائي فوسفات الأمونيوم: فوسفات ثنائي الأمونيوم ( DAP ؛ IUPAC اسم فوسفات هيدروجين ثنائي الأمونيوم ؛ الصيغة الكيميائية (NH 4 ) 2 (HPO 4 ) هي واحدة من سلسلة أملاح فوسفات الأمونيوم القابلة للذوبان في الماء والتي يمكن إنتاجها عندما تتفاعل الأمونيا مع حمض الفوسفوريك. ضغط تفكك الأمونيا على النحو الوارد في التعبير والمعادلة التالية:
|  |
| هيدرو كبريتيد الأمونيوم: هيدرو كبريتيد الأمونيوم هو مركب كيميائي له الصيغة (NH 4 ) HS. |  |
| هيدرو كبريتيد الأمونيوم: هيدرو كبريتيد الأمونيوم هو مركب كيميائي له الصيغة (NH 4 ) HS. |  |
| محلول الأمونيا: محلول الأمونيا، المعروف أيضا باسم المياه الأمونيا، وهيدروكسيد الأمونيوم، الخمور نشادرية، الخمور الأمونيا، ماء النشادر، والأمونيا مائي، أو (غير دقيق) الأمونيا، هو حل من الأمونيا في الماء. يمكن الإشارة إليه بالرموز NH 3 (aq). على الرغم من أن هيدروكسيد الأمونيوم اسم يدل على وجود القلويات مع تكوين [NH 4 +] [OH -]، فإنه من المستحيل فعليا لعينات عزل من NH 4 OH. الأيونات NH 4 + وOH - لا تمثل جزءا كبيرا من المبلغ الإجمالي من الأمونيا إلا في الحلول المخففة للغاية. | |
| الأمونيوم بيتومينوسولفونات: الأمونيوم بيتومينوسولفونات أو بيتومينوسولفونات الأمونيوم هو منتج من أصل طبيعي يتم الحصول عليه في الخطوة الأولى بالتقطير الجاف للصخر الزيتي الغني بالكبريت. عن طريق السلفنة للزيت الناتج ، والمعادلة اللاحقة بالأمونيا ، ينتج Ichthammol كمادة لزجة قابلة للذوبان في الماء لها رائحة مميزة تشبه البيتومين. يستخدم في الطب كعلاج لأمراض الجلد المختلفة ، بما في ذلك الأكزيما والصدفية. المراهم التي تحتوي على 10٪ أو 20٪ Ichthammol هي الأكثر شيوعًا. يطلق عليهم أحيانًا اسم "المراهم السوداء" أو "مرهم الرسم". تم الترويج لعمل Ichthammol الجلدي من قبل الطبيب الألماني Paul Gerson Unna. |  |
| نيتروجين الخميرة: نيتروجين الخميرة أو YAN هو مزيج من النيتروجين الأميني الحر (FAN) والأمونيا (NH 3 ) والأمونيوم (NH 4 + ) المتاح لخميرة النبيذ Saccharomyces cerevisiae لاستخدامه أثناء التخمير. بعيدًا عن السكريات القابلة للتخمير ، الجلوكوز والفركتوز ، يعد النيتروجين أهم العناصر الغذائية اللازمة لإجراء عملية تخمير ناجحة لا تنتهي قبل نقطة الجفاف المقصودة أو تشهد تطور الروائح الكريهة وأعطال النبيذ ذات الصلة. إلى هذا الحد ، غالبًا ما يكمل صانعو النبيذ موارد YAN المتاحة بإضافات النيتروجين مثل فوسفات ثنائي الأمونيوم (DAP). |  |
| يودات الأمونيوم: يودات الأمونيوم عبارة عن ملح غير عضوي قابل للذوبان بشكل ضئيل في البرد ، وقابل للذوبان بشكل معتدل في الماء الساخن ، مثل جميع أملاح اليود ، وهو مؤكسد قوي. |  |
| يوديد الأمونيوم: يوديد الأمونيوم هو المركب الكيميائي NH 4 I. ويستخدم في المواد الكيميائية الفوتوغرافية وبعض الأدوية. يمكن تحضيره عن طريق عمل حمض الهيدرويوديك على الأمونيا. قابل للذوبان في الماء بسهولة ، حيث يتبلور في مكعبات. كما أنه قابل للذوبان في الإيثانول. يتحول تدريجياً إلى اللون الأصفر عند الوقوف في الهواء الرطب ، بسبب التحلل مع تحرير اليود. |  |
| الأمونيوم: كاتيون الأمونيوم هو أيون متعدد الذرات موجب الشحنة مع الصيغة الكيميائية NH + |  |
| كبريتات حديد الأمونيوم (II): كبريتات حديد الأمونيوم (II) ، أو ملح Mohr ، هو مركب غير عضوي له الصيغة (NH 4 ) 2 Fe (SO 4 ) 2 (H 2 O) 6 . تحتوي على كاتيونات مختلفة ، Fe 2+ و NH 4 + ، وتصنف على أنها ملح مزدوج من كبريتات الحديدوز وكبريتات الأمونيوم. إنه كاشف معمل شائع لأنه يتبلور بسهولة ، والبلورات تقاوم الأكسدة عن طريق الهواء. مثل أملاح الكبريتات الحديدية الأخرى ، تذوب كبريتات الأمونيوم الحديدية في الماء لتعطي المركب المائي [Fe (H 2 O) 6 ] 2+ ، الذي له هندسة جزيئية ثماني السطوح. شكله المعدني هو موهريت. | 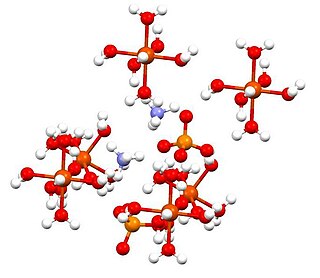 |
| كبريتات حديد الأمونيوم (II): كبريتات حديد الأمونيوم (II) ، أو ملح Mohr ، هو مركب غير عضوي له الصيغة (NH 4 ) 2 Fe (SO 4 ) 2 (H 2 O) 6 . تحتوي على كاتيونات مختلفة ، Fe 2+ و NH 4 + ، وتصنف على أنها ملح مزدوج من كبريتات الحديدوز وكبريتات الأمونيوم. إنه كاشف معمل شائع لأنه يتبلور بسهولة ، والبلورات تقاوم الأكسدة عن طريق الهواء. مثل أملاح الكبريتات الحديدية الأخرى ، تذوب كبريتات الأمونيوم الحديدية في الماء لتعطي المركب المائي [Fe (H 2 O) 6 ] 2+ ، الذي له هندسة جزيئية ثماني السطوح. شكله المعدني هو موهريت. |  |
| كبريتات حديد الأمونيوم (III): كبريتات حديد الأمونيوم (III) ، NH 4 Fe (SO 4 ) 2 · 12 H 2 O ، أو NH 4 [Fe (H 2 O) 6 ] (SO 4 ) 2 · 6 H 2 O ، المعروف أيضًا باسم كبريتات الأمونيوم الحديديك (FAS) أو شب الحديد ، هو ملح مزدوج في فئة الشب ، والذي يتكون من مركبات لها الصيغة العامة AB (SO 4 ) 2 · 12 H 2 O. وله مظهر بلورات ذات لون بنفسجي ضعيف ، بلورات ثماني الأوجه. كان هناك بعض النقاش حول أصل لون البلورات ، حيث عزا البعض ذلك إلى الشوائب في المركب ، وزعم البعض الآخر أنه من خصائص البلورة نفسها. |  |
| سترات الأمونيوم الحديديك: سيترات الأمونيوم الحديديك لها الصيغة (NH 4 ) 5 [Fe (C 6 H 4 O 7 ) 2 ]. السمة المميزة لهذا المركب هي أنه قابل للذوبان في الماء بشكل كبير ، على عكس سترات الحديديك غير القابلة للذوبان بشكل كبير. |  |
| كبريتات حديد الأمونيوم (II): كبريتات حديد الأمونيوم (II) ، أو ملح Mohr ، هو مركب غير عضوي له الصيغة (NH 4 ) 2 Fe (SO 4 ) 2 (H 2 O) 6 . تحتوي على كاتيونات مختلفة ، Fe 2+ و NH 4 + ، وتصنف على أنها ملح مزدوج من كبريتات الحديدوز وكبريتات الأمونيوم. إنه كاشف معمل شائع لأنه يتبلور بسهولة ، والبلورات تقاوم الأكسدة عن طريق الهواء. مثل أملاح الكبريتات الحديدية الأخرى ، تذوب كبريتات الأمونيوم الحديدية في الماء لتعطي المركب المائي [Fe (H 2 O) 6 ] 2+ ، الذي له هندسة جزيئية ثماني السطوح. شكله المعدني هو موهريت. |  |
| كبريتات حديد الأمونيوم (II): كبريتات حديد الأمونيوم (II) ، أو ملح Mohr ، هو مركب غير عضوي له الصيغة (NH 4 ) 2 Fe (SO 4 ) 2 (H 2 O) 6 . تحتوي على كاتيونات مختلفة ، Fe 2+ و NH 4 + ، وتصنف على أنها ملح مزدوج من كبريتات الحديدوز وكبريتات الأمونيوم. إنه كاشف معمل شائع لأنه يتبلور بسهولة ، والبلورات تقاوم الأكسدة عن طريق الهواء. مثل أملاح الكبريتات الحديدية الأخرى ، تذوب كبريتات الأمونيوم الحديدية في الماء لتعطي المركب المائي [Fe (H 2 O) 6 ] 2+ ، الذي له هندسة جزيئية ثماني السطوح. شكله المعدني هو موهريت. |  |
| لاكتات الأمونيوم: لاكتات الأمونيوم مركب له الصيغة NH 4 (C 2 H 4 (OH) COO). إنه ملح الأمونيوم لحمض اللبنيك. لها خصائص مضادة للبكتيريا خفيفة. | 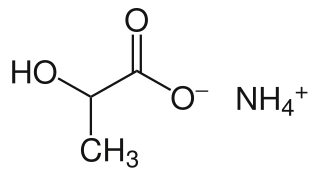 |
| كبريتات الأمونيوم لوريل: كبريتات لوريل الأمونيوم (ALS) هو الاسم الشائع لكبريتات الأمونيوم دوديسيل (CH 3 (CH 2 ) 10 CH 2 OSO 3 NH 4 ). يتكون الأنيون من سلسلة هيدروكربونية غير قطبية ومجموعة نهائية قطبية للكبريتات. يمنح الجمع بين المجموعات غير القطبية والمجموعات القطبية خصائص الفاعل بالسطح للأنيون: فهو يسهل انحلال كل من المواد القطبية وغير القطبية. يصنف ALS على أنه إستر كبريتات. يوجد بشكل أساسي في الشامبو وغسول الجسم كعامل رغوة. / كبريتات لوريل هي مواد خافضة للتوتر السطحي عالية الرغوة تعطل التوتر السطحي للماء جزئيًا عن طريق تكوين المذيلات في واجهة الهواء السطحي. | |
| ستروفيت: الستروفيت (فوسفات الأمونيوم المغنيسيوم) هو معدن فوسفاتي بالصيغة: NH 4 MgPO 4 · 6H 2 O. يتبلور الستروفيت في نظام تقويم العظام على شكل بلورات هرمية بيضاء إلى صفراء أو بيضاء بنية أو في أشكال تشبه الميكا. إنه معدن ناعم بصلابة موس من 1.5 إلى 2 وله ثقل نوعي منخفض يبلغ 1.7. إنه قابل للذوبان بشكل ضئيل في الظروف المحايدة والقلوية ، ولكنه قابل للذوبان بسهولة في الحمض. |  |
| Boussingaultite: Boussingaultite هو معدن كبريتات نادر له الصيغة الكيميائية: (NH 4 ) 2 Mg (SO 4 ) 2 · 6 (H 2 O). صيغة boussingaultite هي تلك الخاصة بنوع أملاح Tutton. تم وصفه في الأصل من حقول الطاقة الحرارية الأرضية في توسكانا بإيطاليا ، حيث يوجد مع موهريت التماثلية الحديدي ، ولكنه يوجد بشكل أكثر شيوعًا في مكبات الفحم المحترقة. يمتلك المعدن تناظرًا أحادي الميل ويشكل بلورات واضحة ومستديرة في كثير من الأحيان. | |
| مالات الأمونيوم: مالات الأمونيوم مركب له الصيغة NH 4 (C 2 H 4 O (COO) 2 ). إنه ملح الأمونيوم لحمض الماليك. يتم استخدامه كمادة مضافة للغذاء وله رقم E E349. |  |
| المنغنيز البنفسجي: المنغنيز البنفسجي هو الاسم الشائع لبيروفوسفات الأمونيوم (III) ، وهو مركب غير عضوي يتكون من الأمونيوم والمنغنيز في حالة الأكسدة +3 ، وأنيون بيروفوسفات. يتم تحضيره عن طريق تسخين خليط من أكسيد المنغنيز (III) ، ثنائي فوسفات ثنائي الأمونيوم وحمض الفوسفوريك. هذه المادة هي صبغة غير عضوية شائعة. |  |
| المنغنيز البنفسجي: المنغنيز البنفسجي هو الاسم الشائع لبيروفوسفات الأمونيوم (III) ، وهو مركب غير عضوي يتكون من الأمونيوم والمنغنيز في حالة الأكسدة +3 ، وأنيون بيروفوسفات. يتم تحضيره عن طريق تسخين خليط من أكسيد المنغنيز (III) ، ثنائي فوسفات ثنائي الأمونيوم وحمض الفوسفوريك. هذه المادة هي صبغة غير عضوية شائعة. |  |
| ميتافانادات الأمونيوم: ميتافانادات الأمونيوم هو مركب غير عضوي مع الصيغة NH 4 VO 3 . إنه ملح أبيض ، على الرغم من أن العينات غالبًا ما تكون صفراء بسبب شوائب V 2 O 5 . وهو وسيط مهم في تنقية الفاناديوم. |  |
| موليبدات الأمونيوم: يمكن أن يكون موليبدات الأمونيوم من أشكال مختلفة. قد يشار إلى هذه:
| |
| موليبدات الأمونيوم: يمكن أن يكون موليبدات الأمونيوم من أشكال مختلفة. قد يشار إلى هذه:
| |
| الأمونيوم هيبتاموليبدات: الأمونيوم heptamolybdate هو مركب غير العضوية التي الصيغة الكيميائية هي (NH 4) 6 مو 7 O 24، واجه عادة باسم tetrahydrate. ثنائي الهيدرات معروف أيضًا. وهي مادة صلبة عديمة اللون ، يشار إليها غالبًا باسم باراموليبدات الأمونيوم أو ببساطة موليبدات الأمونيوم ، على الرغم من أن "موليبدات الأمونيوم" يمكن أن يشير أيضًا إلى أورثوموليبدات الأمونيوم ، (NH 4 ) 2 MoO 4 ، والعديد من المركبات الأخرى. إنه أحد أكثر مركبات الموليبدينوم شيوعًا. |  |
| ثنائي فوسفات الأمونيوم: فوسفات ثنائي الأمونيوم ( DAP ؛ IUPAC اسم فوسفات هيدروجين ثنائي الأمونيوم ؛ الصيغة الكيميائية (NH 4 ) 2 (HPO 4 ) هي واحدة من سلسلة أملاح فوسفات الأمونيوم القابلة للذوبان في الماء والتي يمكن إنتاجها عندما تتفاعل الأمونيا مع حمض الفوسفوريك. ضغط تفكك الأمونيا على النحو الوارد في التعبير والمعادلة التالية:
|  |
| حمض الموسيك: حمض Mucic ، C 6 H 10 O 8 أو HOOC- (CHOH) 4- COOH (المعروف أيضًا باسم حمض الجلاكتاريك أو حمض الجلاكتاريك المتوسط ) هو حمض الداريك الذي يتم الحصول عليه عن طريق أكسدة حمض النيتريك في الجلاكتوز أو المركبات المحتوية على الجلاكتوز مثل اللاكتوز ، الدولسيت. ، وكويرسايت ، ومعظم أنواع العلكة. |  |
| كلوريد الأمونيوم: كلوريد الأمونيوم مركب غير عضوي مع الصيغة NH 4 Cl وملح بلوري أبيض قابل للذوبان في الماء بدرجة عالية. محاليل كلوريد الأمونيوم حمضية بشكل معتدل. Sal ammoniac هو اسم للشكل الطبيعي والمعدني لكلوريد الأمونيوم. يتكون المعدن بشكل شائع عند حرق مقالب الفحم من تكثيف الغازات المشتقة من الفحم. يوجد أيضًا حول بعض أنواع الفتحات البركانية. يستخدم بشكل أساسي كسماد وعامل توابل في بعض أنواع عرق السوس. إنه ناتج عن تفاعل حمض الهيدروكلوريك والأمونيا. |  |
| ملح توتون: أملاح توتون هي عائلة من الأملاح بالصيغة M 2 M '(SO 4 ) 2 (H 2 O) 6 (كبريتات) أو M 2 M' (SeO 4 ) 2 (H 2 O) 6 (سيلينات). هذه المواد عبارة عن أملاح مزدوجة ، مما يعني أنها تحتوي على كاتيونيين مختلفين ، M + و M ' 2+ متبلوران في نفس الشبكة الأيونية العادية. يمكن أن يكون الكاتيون أحادي التكافؤ عبارة عن بوتاسيوم ، روبيديوم ، سيزيوم ، أمونيوم (NH 4 ) ، أمونيوم منزوع الدوتر (ND 4 ) أو ثاليوم. أيونات الصوديوم أو الليثيوم صغيرة جدًا. يمكن أن يكون الكاتيون ثنائي التكافؤ عبارة عن المغنيسيوم أو الفاناديوم أو الكروم أو المنغنيز أو الحديد أو الكوبالت أو النيكل أو النحاس أو الزنك أو الكادميوم. بالإضافة إلى كبريتات وselenate، يمكن للأنيون ثنائي التكافؤ يكون كرومات (CRO 4 2-)، tetrafluoroberyllate (BEF 4 2-)، hydrogenphosphate (HPO 4 2-) أو مونوفلووروبهوسبهاتي (أ ف ب 3 F 2-). تتبلور أملاح توتون في المجموعة الفضائية أحادية الميل P 2 1 / a . القوة هي نتيجة الرابطة الهيدروجينية التكميلية بين الأنيونات الرباعية السطوح والكاتيونات بالإضافة إلى تفاعلها مع المركب المعدني المائي [M (H 2 O) 6 ] 2+ . | |
| نترات الأمونيوم: نترات الأمونيوم مركب كيميائي له الصيغة الكيميائية NH 4 لا 3 . وهو مادة صلبة بلورية بيضاء تتكون من أيونات الأمونيوم والنترات. إنه قابل للذوبان بدرجة عالية في الماء ومرطب كمادة صلبة ، على الرغم من أنه لا يشكل هيدرات. يستخدم في الغالب في الزراعة كسماد عالي النيتروجين. قُدر الإنتاج العالمي بنحو 21.6 مليون طن في عام 2017. |  |
| ANFO: ANFO هي مادة متفجرة صناعية سائبة تستخدم على نطاق واسع. يتم نطق اسمها بشكل شائع باسم " ANN-foe " . |  |
| قائمة كوارث نترات الأمونيوم: عند تسخينها ، تتحلل نترات الأمونيوم بشكل غير قابل للانفجار إلى غازات من الأكسجين والنيتروجين وبخار الماء ؛ ومع ذلك ، يمكن حثه على التحلل بشكل متفجر عن طريق التفجير إلى أكسيد النيتروز وبخار الماء. يمكن أن تشكل المخزونات الكبيرة من المواد خطر نشوب حريق كبير بسبب الأكسدة الداعمة لها ، وقد تنفجر أيضًا ، كما حدث في كارثة مدينة تكساس عام 1947 والتي أدت إلى تغييرات كبيرة في لوائح التخزين والمناولة. | |
| قائمة كوارث نترات الأمونيوم: عند تسخينها ، تتحلل نترات الأمونيوم بشكل غير قابل للانفجار إلى غازات من الأكسجين والنيتروجين وبخار الماء ؛ ومع ذلك ، يمكن حثه على التحلل بشكل متفجر عن طريق التفجير إلى أكسيد النيتروز وبخار الماء. يمكن أن تشكل المخزونات الكبيرة من المواد خطر نشوب حريق كبير بسبب الأكسدة الداعمة لها ، وقد تنفجر أيضًا ، كما حدث في كارثة مدينة تكساس عام 1947 والتي أدت إلى تغييرات كبيرة في لوائح التخزين والمناولة. | |
| نترات الأمونيوم: نترات الأمونيوم مركب كيميائي له الصيغة الكيميائية NH 4 لا 3 . وهو مادة صلبة بلورية بيضاء تتكون من أيونات الأمونيوم والنترات. إنه قابل للذوبان بدرجة عالية في الماء ومرطب كمادة صلبة ، على الرغم من أنه لا يشكل هيدرات. يستخدم في الغالب في الزراعة كسماد عالي النيتروجين. قُدر الإنتاج العالمي بنحو 21.6 مليون طن في عام 2017. |  |
| نترات الأمونيوم: نترات الأمونيوم مركب كيميائي له الصيغة الكيميائية NH 4 لا 3 . وهو مادة صلبة بلورية بيضاء تتكون من أيونات الأمونيوم والنترات. إنه قابل للذوبان بدرجة عالية في الماء ومرطب كمادة صلبة ، على الرغم من أنه لا يشكل هيدرات. يستخدم في الغالب في الزراعة كسماد عالي النيتروجين. قُدر الإنتاج العالمي بنحو 21.6 مليون طن في عام 2017. |  |
| الأمونيا: الأمونيا مركب من النيتروجين والهيدروجين بالصيغة NH 3 . هيدريد ثنائي مستقر ، وأبسط هيدريد البنيكتوجين ، الأمونيا هو غاز عديم اللون له خاصية مميزة للرائحة النفاذة. إنها نفايات نيتروجينية شائعة ، خاصة بين الكائنات المائية ، وتساهم بشكل كبير في الاحتياجات الغذائية للكائنات الأرضية من خلال كونها مقدمة للأغذية والأسمدة. الأمونيا ، بشكل مباشر أو غير مباشر ، هي أيضًا لبنة لبناء العديد من المنتجات الصيدلانية وتستخدم في العديد من منتجات التنظيف التجارية. يتم جمعها بشكل أساسي عن طريق الإزاحة الهبوطية لكل من الهواء والماء. |  |
| نتريت الأمونيوم: نتريت الأمونيوم NH 4 NO 2 هو ملح الأمونيوم لحمض النيتروز. لا يتم استخدامه في شكل منعزل نقي لأنه غير مستقر للغاية ويتحلل في الماء والنيتروجين ، حتى في درجة حرارة الغرفة. |  |
| نونوات الأمونيوم: نونوات الأمونيوم هو مبيد أعشاب غير جهازي واسع الطيف ليس له نشاط في التربة. يمكن استخدامه لقمع الحشائش ومكافحتها ، بما في ذلك الأعشاب والكروم والنباتات الشجرية والنباتات السنوية / المعمرة ، بما في ذلك الطحالب والشتلات ومصاصي الأشجار. يتم تسويق nonanoate الأمونيوم كحلول مائية. في درجة حرارة الغرفة عند أقصى تركيز في الماء (40٪). المحاليل عديمة اللون إلى سائل أصفر باهت برائحة حامض دهني خفيف. إنه مستقر في التخزين. يوجد نونوات الأمونيوم في شكل بلورات بيضاء. | |
| أورثوموليبدات الأمونيوم: أورثوموليبدات الأمونيوم هو مركب غير عضوي له الصيغة الكيميائية (NH 4 ) 2 MoO 4 . وهي مادة صلبة بيضاء يتم تحضيرها بمعالجة ثالث أكسيد الموليبدينوم مع الأمونيا المائية. عند تسخين هذه الحلول، يتم فقدان الأمونيا، لإعطاء موليبدات أمونيوم ((NH 4) 6 مو 7 O 24. 4H 2 O). يستخدم orthomolybdate الأمونيوم كمثبط للتآكل وهو وسيط في بعض المخططات لكسب الموليبدينوم من خاماته. | |
| أكسالات الأمونيوم: أكسالات الأمونيوم ، C 2 H 8 N 2 O 4 - يكتب بشكل أكثر شيوعًا كـ (NH 4 ) 2 C 2 O 4 - عبارة عن ملح أكسالات مع الأمونيوم (أحيانًا على شكل أحادي الهيدرات). وهو ملح عديم اللون (أبيض) في ظل الظروف القياسية وهو عديم الرائحة وغير متطاير. وهو ملح الأمونيوم لحمض الأكساليك ، ويوجد في العديد من النباتات والخضروات. | 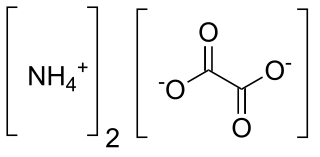 |
| الأمونيوم هيبتاموليبدات: الأمونيوم heptamolybdate هو مركب غير العضوية التي الصيغة الكيميائية هي (NH 4) 6 مو 7 O 24، واجه عادة باسم tetrahydrate. ثنائي الهيدرات معروف أيضًا. وهي مادة صلبة عديمة اللون ، يشار إليها غالبًا باسم باراموليبدات الأمونيوم أو ببساطة موليبدات الأمونيوم ، على الرغم من أن "موليبدات الأمونيوم" يمكن أن يشير أيضًا إلى أورثوموليبدات الأمونيوم ، (NH 4 ) 2 MoO 4 ، والعديد من المركبات الأخرى. إنه أحد أكثر مركبات الموليبدينوم شيوعًا. |  |
| الأمونيوم paratungstate: الأمونيوم paratungstate (أو APT) هو ملح أبيض بلوري مع الصيغة الكيميائية (NH 4 ) 10 (H 2 W 12 O 42 ) · 4H 2 O. يوصف بأنه "أهم مادة خام لمنتجات التنجستن الأخرى." |  |
| نونوات الأمونيوم: نونوات الأمونيوم هو مبيد أعشاب غير جهازي واسع الطيف ليس له نشاط في التربة. يمكن استخدامه لقمع الحشائش ومكافحتها ، بما في ذلك الأعشاب والكروم والنباتات الشجرية والنباتات السنوية / المعمرة ، بما في ذلك الطحالب والشتلات ومصاصي الأشجار. يتم تسويق nonanoate الأمونيوم كحلول مائية. في درجة حرارة الغرفة عند أقصى تركيز في الماء (40٪). المحاليل عديمة اللون إلى سائل أصفر باهت برائحة حامض دهني خفيف. إنه مستقر في التخزين. يوجد نونوات الأمونيوم في شكل بلورات بيضاء. | |
| فوق كلورات الأمونيوم: فوق كلورات الأمونيوم ("AP") مركب غير عضوي له الصيغة NH 4 ClO 4 . وهي مادة صلبة عديمة اللون أو بيضاء قابلة للذوبان في الماء. إنه مؤكسد قوي. إلى جانب الوقود ، يمكن استخدامه كوقود دفع للصواريخ. تسبب عدم استقرارها في وقوع عدد من الحوادث ، مثل كارثة PEPCON. |  |
| دافع مركب فوق كلورات الأمونيوم: الوقود المركب فوق كلورات الأمونيوم ( APCP ) هو وقود حديث يستخدم في المركبات الصاروخية التي تعمل بالوقود الصلب. إنه يختلف عن العديد من الوقود التقليدي للصواريخ الصلبة مثل المسحوق الأسود أو كبريت الزنك ، ليس فقط في التركيب الكيميائي والأداء العام ولكن أيضًا في طبيعة كيفية معالجته. يتم صب APCP في الشكل ، على عكس مسحوق المسحوق كما هو الحال مع المسحوق الأسود. يوفر هذا انتظام التصنيع والتكرار ، وهما متطلبات ضرورية للاستخدام في صناعة الطيران. | |
| الأمونيوم بيرفلورونونوات: الأمونيوم المشبع بالفلورونونوات ( APFN ) هو عامل خافض للتوتر السطحي أنيوني يشكل مراحل بلورية سائلة في الماء. إنه ملح الأمونيوم لحمض البيرفلورونونويك. | |
| حمض البيرفلوروكتانويك: حمض البيرفلوروكتانويك ( PFOA ) - المعروف أيضًا بالعامية باسم C8 - عبارة عن حمض كربوكسيل مشبع بالفلور يتم إنتاجه واستخدامه في جميع أنحاء العالم كخافض للتوتر السطحي الصناعي في العمليات الكيميائية وكمواد وسيطة. وهو نتاج مخاوف صحية ويخضع لإجراءات تنظيمية وللتخلص التدريجي الصناعي الطوعي. يعتبر حمض بيرفلورو الأوكتانول خافض للتوتر السطحي ، أو خافض للتوتر السطحي ، بسبب تركيبته الكيميائية ، والتي تتكون من "مجموعة ذيل" مشبعة بالفلور ، n -octyl و carboxylate "مجموعة رأس". يمكن وصف مجموعة الرأس بأنها محبة للماء بينما ذيل الفلوروكربون كاره للماء ومضاد للدهون. مجموعة الذيل خاملة ولا تتفاعل بقوة مع الشقوق الكيميائية القطبية أو غير القطبية ؛ مجموعة الرأس تفاعلية وتتفاعل بقوة مع المجموعات القطبية ، وتحديداً الماء. "الذيل" كاره للماء نظرًا لكونه غير قطبي ومضاد للدهون لأن مركبات الكربون الفلورية أقل عرضة لقوة تشتت لندن من الهيدروكربونات. |  |
| برمنجنات الأمونيوم: برمنجنات الأمونيوم هو مركب كيميائي NH 4 MnO 4 ، أو NH 3 · HMnO 4 . وهو ملح قابل للذوبان في الماء ، بني بنفسجي أو بنفسجي غامق. إنه مؤكسد قوي ، بسبب أنيون البرمنجنات ، وهو مادة متفجرة قوية إلى حد ما ، بسبب مزيج أنيون برمنجنات المؤكسد وتقليل كاتيون الأمونيوم. يمكن أن تنفجر برمنجنات الأمونيوم الجافة عن طريق الحرارة أو الصدمة أو الاحتكاك ، وقد تنفجر عند درجات حرارة أعلى من 140 درجة فهرنهايت (60 درجة مئوية). |  |
| بيرسلفات الأمونيوم: بيرسلفات الأمونيوم (APS) هو مركب غير عضوي له الصيغة (NH 4 ) 2 S 2 O 8 . إنه ملح عديم اللون (أبيض) قابل للذوبان في الماء بدرجة كبيرة ، أكثر بكثير من ملح البوتاسيوم المرتبط به. إنه عامل مؤكسد قوي يستخدم في كيمياء البوليمر ، كعامل تنظيف وتبييض. |  |
| بيرسلفات الأمونيوم: بيرسلفات الأمونيوم (APS) هو مركب غير عضوي له الصيغة (NH 4 ) 2 S 2 O 8 . إنه ملح عديم اللون (أبيض) قابل للذوبان في الماء بدرجة كبيرة ، أكثر بكثير من ملح البوتاسيوم المرتبط به. إنه عامل مؤكسد قوي يستخدم في كيمياء البوليمر ، كعامل تنظيف وتبييض. |  |
| الأمونيوم بيررينات: الأمونيوم perrhenate (APR) هو ملح الأمونيوم لحمض بيررينيك NH 4 ReO 4 . إنه الشكل الأكثر شيوعًا الذي يتم فيه تداول الرينيوم. إنه ملح أبيض قابل للذوبان في الماء. تم وصفه لأول مرة بعد وقت قصير من اكتشاف الرينيوم. | 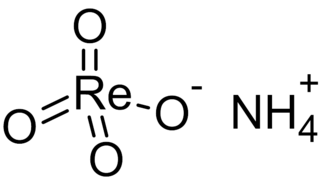 |
| الأمونيوم بيررينات: الأمونيوم perrhenate (APR) هو ملح الأمونيوم لحمض بيررينيك NH 4 ReO 4 . إنه الشكل الأكثر شيوعًا الذي يتم فيه تداول الرينيوم. إنه ملح أبيض قابل للذوبان في الماء. تم وصفه لأول مرة بعد وقت قصير من اكتشاف الرينيوم. |  |
| بيرسلفات الأمونيوم: بيرسلفات الأمونيوم (APS) هو مركب غير عضوي له الصيغة (NH 4 ) 2 S 2 O 8 . إنه ملح عديم اللون (أبيض) قابل للذوبان في الماء بدرجة كبيرة ، أكثر بكثير من ملح البوتاسيوم المرتبط به. إنه عامل مؤكسد قوي يستخدم في كيمياء البوليمر ، كعامل تنظيف وتبييض. |  |
| بيرسلفات الأمونيوم: بيرسلفات الأمونيوم (APS) هو مركب غير عضوي له الصيغة (NH 4 ) 2 S 2 O 8 . إنه ملح عديم اللون (أبيض) قابل للذوبان في الماء بدرجة كبيرة ، أكثر بكثير من ملح البوتاسيوم المرتبط به. إنه عامل مؤكسد قوي يستخدم في كيمياء البوليمر ، كعامل تنظيف وتبييض. |  |
| الأمونيوم بيرتكنيتات: الأمونيوم بيرتكنيتات هو مركب كيميائي له الصيغة NH 4 TcO 4 . إنه ملح الأمونيوم لحمض البيرتيكنيك. يستخدم الشكل الأكثر شيوعًا 99 Tc . المركب قابل للذوبان بسهولة في المحاليل المائية التي تشكل أيونات الأمونيوم والبيرتكنيتات. |  |
| فوسفات الامونيوم: فوسفات الأمونيوم هو مركب غير عضوي بالصيغة (NH 4 ) 3 PO 4 . إنه ملح الأمونيوم لحمض الفوسفوريك. "ملح مزدوج" ذي صلة ، (NH 4 ) 3 PO 4 . (NH 4 ) 2 HPO 4 معترف به أيضًا ولكنه استخدام غير عملي. كل من أملاح التريامونيوم تطور الأمونيا. على النقيض من الطبيعة غير المستقرة لأملاح التريامونيوم ، فإن ثنائي فوسفات ثنائي الأمونيوم (NH 4 ) 2 HPO 4 وملح أحادي الأمونيوم (NH 4 ) H 2 PO 4 هي مواد ثابتة تستخدم بشكل شائع كأسمدة لتزويد النباتات بالنيتروجين والفوسفور الثابت. |  |
| فوسفات الأمونيوم (مركبات): يشير فوسفات الأمونيوم إلى ثلاثة مركبات كيميائية مختلفة ، تتشكل جميعها عن طريق تفاعل الأمونيا مع حمض الفوسفوريك ولها الصيغة العامة [NH 4 ] x [H 3 x PO 4 ] ، حيث 1 x ≤ 3:
| |
| فوسفات الامونيوم: فوسفات الأمونيوم هو مركب غير عضوي بالصيغة (NH 4 ) 3 PO 4 . إنه ملح الأمونيوم لحمض الفوسفوريك. "ملح مزدوج" ذي صلة ، (NH 4 ) 3 PO 4 . (NH 4 ) 2 HPO 4 معترف به أيضًا ولكنه استخدام غير عملي. كل من أملاح التريامونيوم تطور الأمونيا. على النقيض من الطبيعة غير المستقرة لأملاح التريامونيوم ، فإن ثنائي فوسفات ثنائي الأمونيوم (NH 4 ) 2 HPO 4 وملح أحادي الأمونيوم (NH 4 ) H 2 PO 4 هي مواد ثابتة تستخدم بشكل شائع كأسمدة لتزويد النباتات بالنيتروجين والفوسفور الثابت. |  |
| أملاح الأمونيوم المختلطة من الجلسريدات الفسفورية: يمكن صنع مزيج أملاح الأمونيوم من الجلسريدات المُفسفرة إما صناعياً أو من خليط من الجلسرين والزيوت النباتية المصلبة جزئياً. | |
| فوسفوموليبدات الأمونيوم: فوسفوموليبدات الأمونيوم هو الملح غير العضوي لحمض الفوسفوموليبدك بالصيغة الكيميائية (NH 4 ) 3 PMo 12 O 40 . يحتوي على مركب أيون الفوسفوموليبدات. |  |
| دونيت: Dunnite ، المعروف أيضًا باسم Explosive D أو بشكل منهجي باسم picrate الأمونيوم ، هو متفجر تم تطويره في عام 1906 من قبل الرائد بالجيش الأمريكي بيفرلي دبليو دن ، الذي شغل فيما بعد منصب كبير المفتشين في مكتب نقل المتفجرات. بيكرات الأمونيوم عبارة عن ملح يتكون من تفاعل حمض البيكريك والأمونيا. يرتبط كيميائياً بـ trinitrotoluene المتفجر الأكثر استقرارًا (TNT). |  |
| دونيت: Dunnite ، المعروف أيضًا باسم Explosive D أو بشكل منهجي باسم picrate الأمونيوم ، هو متفجر تم تطويره في عام 1906 من قبل الرائد بالجيش الأمريكي بيفرلي دبليو دن ، الذي شغل فيما بعد منصب كبير المفتشين في مكتب نقل المتفجرات. بيكرات الأمونيوم عبارة عن ملح يتكون من تفاعل حمض البيكريك والأمونيا. يرتبط كيميائياً بـ trinitrotoluene المتفجر الأكثر استقرارًا (TNT). |  |
| سداسي كلورو بلاتينات الأمونيوم: سداسي كلورو بلاتينات الأمونيوم ، المعروف أيضًا باسم كلوروبلاتينات الأمونيوم ، هو مركب غير عضوي له الصيغة (NH 4 ) 2 [PtCl 6 ]. إنه مثال نادر لملح البلاتين (IV) القابل للذوبان غير المرطب. يشكل محاليل صفراء مكثفة في الماء. في وجود 1M NH 4 Cl ، تكون قابليته للذوبان 0.0028 جم / 100 مل. |  |
| الأمونيوم متعدد الفوسفات: الأمونيوم متعدد الفوسفات هو ملح غير عضوي لحمض عديد الفوسفوريك والأمونيا يحتوي على كلا السلاسل وربما المتفرعة. تركيبته الكيميائية هي [NH 4 PO 3] ن (OH) 2 تبين أن كل مونومر يتكون من راديكالية الفوسفاتية من ذرة فوسفور مع ثلاثة الأكسجين وشحنة سالبة واحدة تحييد قبل الموجبة الأمونيوم ترك اثنين من السندات تتردد في بلمرة. في الحالات المتفرعة ، تفتقد بعض المونومرات لأنيون الأمونيوم وبدلاً من ذلك ترتبط بثلاثة مونومرات أخرى. |  |
| بروبيونات الأمونيوم: بروبيونات الأمونيوم أو بروبونات الأمونيوم هو ملح الأمونيوم لحمض البروبيونيك. لها الصيغة الكيميائية NH 4 (C 2 H 5 COO). |  |
| موركسايد: الموريكسيد (NH 4 C 8 H 4 N 5 O 6 ، أو C 8 H 5 N 5 O 6 · NH 3 ) ، ويسمى أيضًا فرفريات الأمونيوم أو MX ، هو ملح الأمونيوم لحمض البربوريك. إنها مادة صلبة أرجوانية قابلة للذوبان في الماء. تم استخدام المركب مرة واحدة كمؤشر كاشف. المحلول المائي أصفر عند درجة الحموضة المنخفضة ، والأرجواني المحمر في المحاليل الحمضية الضعيفة ، والأزرق البنفسجي في المحاليل القلوية. |  |
| ثاني كرومات الأمونيوم: ثنائي كرومات الأمونيوم مركب غير عضوي بالصيغة (NH 4 ) 2 Cr 2 O 7 . في هذا المركب ، كما هو الحال في جميع الكرومات وثنائي كرومات ، يكون الكروم في حالة أكسدة +6 ، والمعروف باسم الكروم سداسي التكافؤ. وهو ملح يتكون من أيونات الأمونيوم وأيونات ثنائي كرومات. |  |
| ديثيوكاربامات بيروليدين: Pyrrolidine dithiocarbamate (PDTC) هي عائلة من الأدوية وثيقة الصلة المستخدمة في عملية إزالة معدن ثقيل ، وتحريض توقف دورة الخلية في المرحلة G1 ، ومنع تحريض سينسيز أكسيد النيتريك. |  |
| ديثيوكاربامات بيروليدين: Pyrrolidine dithiocarbamate (PDTC) هي عائلة من الأدوية وثيقة الصلة المستخدمة في عملية إزالة معدن ثقيل ، وتحريض توقف دورة الخلية في المرحلة G1 ، ومنع تحريض سينسيز أكسيد النيتريك. |  |
| ملح Reinecke: ملح Reinecke مركب كيميائي له الصيغة NH 4 [Cr (NCS) 4 (NH 3 ) 2 ] · H 2 O. المركب البلوري ذو اللون الأحمر الداكن قابل للذوبان في الماء المغلي والأسيتون والإيثانول. ذرة الكروم محاطة بستة ذرات نيتروجين في هندسة ثماني السطوح. تكون روابط NH 3 عابرة بشكل متبادل ومجموعات Cr-NCS خطية. يتبلور الملح مع جزيء واحد من الماء. |  |
| الأمونيوم: كاتيون الأمونيوم هو أيون متعدد الذرات موجب الشحنة مع الصيغة الكيميائية NH + |  |
| سيلينيد الأمونيوم: سيلينيد الأمونيوم مركب كيميائي برمز (NH 4 ) 2 Se. تم الإبلاغ عن العديد من التوليفات ولكن لم يتم تأكيدها. لقد تم تصنيعه عن طريق تفاعل الأمونيا مع سيلينيد الهيدروجين. | |
| الأمونيوم فلوروسيليكات: فلوروسيليكات الأمونيوم (المعروف أيضًا باسم سداسي فلوروسيليكات الأمونيوم أو فلوسيليكات الأمونيوم أو سيليكوفلوريد الأمونيوم) له الصيغة (NH 4 ) 2 SiF 6 . إنها مادة كيميائية سامة ، مثل جميع أملاح حمض الفلوروسيليك. وهي مصنوعة من بلورات بيضاء ، والتي لها ما لا يقل عن ثلاثة أشكال متعددة وتظهر في الطبيعة كمعادن نادرة كريبتوهاليت أو باراريت. |  |
| الأمونيوم فلوروسيليكات: فلوروسيليكات الأمونيوم (المعروف أيضًا باسم سداسي فلوروسيليكات الأمونيوم أو فلوسيليكات الأمونيوم أو سيليكوفلوريد الأمونيوم) له الصيغة (NH 4 ) 2 SiF 6 . إنها مادة كيميائية سامة ، مثل جميع أملاح حمض الفلوروسيليك. وهي مصنوعة من بلورات بيضاء ، والتي لها ما لا يقل عن ثلاثة أشكال متعددة وتظهر في الطبيعة كمعادن نادرة كريبتوهاليت أو باراريت. |  |
| كبريتات الأمونيوم: كبريتات الأمونيوم مادة صلبة بلورية بيضاء ، قابلة للذوبان في الماء بسهولة. يستخدم بشكل شائع كمبيد أعشاب واسع الطيف ، مع استخدامات إضافية كمسرع للسماد ، ومثبط للهب ، وفي العمليات الصناعية. |  |
| كبريتات الامونيوم: كبريتات الأمونيوم (الإنجليزية الأمريكية والاستخدام العلمي الدولي ؛ كبريتات الأمونيوم باللغة الإنجليزية البريطانية) ؛ (NH 4 ) 2 SO 4 هو ملح غير عضوي له عدد من الاستخدامات التجارية. الاستخدام الأكثر شيوعًا هو كسماد التربة. يحتوي على 21٪ نيتروجين و 24٪ كبريت. | 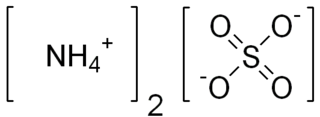 |
| كبريتات الأمونيوم ترسيب: يعتبر ترسيب كبريتات الأمونيوم أحد أكثر الطرق شيوعًا لتنقية البروتينات الكبيرة والمخبرية وتجزئتها والتي يمكن استخدامها لفصل البروتينات عن طريق تغيير قابليتها للذوبان في وجود تركيز عالٍ من الملح. | |
| هيدرو كبريتيد الأمونيوم: هيدرو كبريتيد الأمونيوم هو مركب كيميائي له الصيغة (NH 4 ) HS. |  |
| كبريتات الأمونيوم: كبريتات الأمونيوم هو ملح الأمونيوم لحمض الكبريتيك بالصيغة الكيميائية (NH 4 ) 2 SO 3 . |  |
| ثيوسيانات الأمونيوم: ثيوسيانات الأمونيوم مركب غير عضوي بالصيغة NH 4 SCN. إنه ملح كاتيون الأمونيوم وأنيون الثيوسيانات. |  |
| ثيوسيانات الأمونيوم: ثيوسيانات الأمونيوم مركب غير عضوي بالصيغة NH 4 SCN. إنه ملح كاتيون الأمونيوم وأنيون الثيوسيانات. |  |
| كبريتات الأمونيوم: كبريتات الأمونيوم مادة صلبة بلورية بيضاء ، قابلة للذوبان في الماء بسهولة. يستخدم بشكل شائع كمبيد أعشاب واسع الطيف ، مع استخدامات إضافية كمسرع للسماد ، ومثبط للهب ، وفي العمليات الصناعية. |  |
بحث هذه المدونة الإلكترونية
الخميس، 10 يونيو 2021
Ceric ammonium nitrate, Ammonium chlorate, Ammonium chloride
الاشتراك في:
تعليقات الرسالة (Atom)
-
علي بن محزيار الأهواز: كان علي بن محزيار الأحوازي عالمًا قضائيًا شيعيًا مبكرًا وبارزًا وراويًا وعالمًا. محزيار عالم من القرن التاسع و...
-
مسجد علي بيتشن: مسجد علي بيتشين أو مسجد Zawj Euyun هو مسجد تاريخي في الجزائر العاصمة ، الجزائر. أمر علي بيتشن ببناء المسجد في عام ...
-
علي فاركا توري: كان علي إبراهيم " علي فركة " توري مغنيًا ماليًا وعازفًا متعدد الآلات ، وأحد أشهر الموسيقيين في القارة الأف...
ليست هناك تعليقات:
إرسال تعليق