| الأسبارتام: الأسبارتام هو مُحلي صناعي خالٍ من السكريات أحلى 200 مرة من السكروز ، ويستخدم عادة كبديل للسكر في الأطعمة والمشروبات. وهو إستر ميثيل لحمض الأسبارتيك / ثنائي ببتيد فينيل ألانين مع الأسماء التجارية NutraSweet و Equal و Canderel . تم تصنيع الأسبارتام لأول مرة في عام 1965 وتمت الموافقة عليه للاستخدام في المنتجات الغذائية من قبل إدارة الغذاء والدواء الأمريكية (FDA) في عام 1981. | 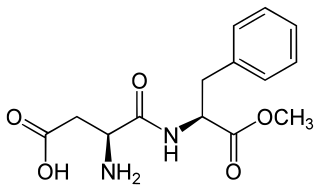 |
| أمينو (التطبيق): Amino هو تطبيق وسائط اجتماعية تم تطويره في الأصل بواسطة Narvii، Inc. وقد تم إنشاؤه في الأصل بواسطة Yin Wang و Ben Anderson في عام 2014. استحوذت MediaLab على Amino في عام 2021 ، ولم يعد المؤسسون مرتبطين بالتطبيق. | |
| أمينو (التطبيق): Amino هو تطبيق وسائط اجتماعية تم تطويره في الأصل بواسطة Narvii، Inc. وقد تم إنشاؤه في الأصل بواسطة Yin Wang و Ben Anderson في عام 2014. استحوذت MediaLab على Amino في عام 2021 ، ولم يعد المؤسسون مرتبطين بالتطبيق. | |
| أمينو (توضيح): أمينو - هو شكل صفة من الأمونيا. | |
| أمينو (اللقب): Amino هو لقب ياباني. الأشخاص البارزون الذين يحملون اللقب هم:
| |
| حمض أميني: الأحماض الأمينية عبارة عن مركبات عضوية تحتوي على مجموعات وظيفية أمينية (–NH 2 ) وكربوكسيل (–COOH) ، جنبًا إلى جنب مع سلسلة جانبية (مجموعة R) خاصة بكل حمض أميني. العناصر الرئيسية للحمض الأميني هي الكربون (C) والهيدروجين (H) والأكسجين (O) والنيتروجين (N) ، على الرغم من وجود عناصر أخرى في السلاسل الجانبية لبعض الأحماض الأمينية. يُعرف حوالي 500 من الأحماض الأمينية التي تحدث بشكل طبيعي اعتبارًا من عام 1983 (على الرغم من ظهور 20 فقط في الشفرة الوراثية) ويمكن تصنيفها بعدة طرق. يمكن تصنيفها وفقًا لمواقع المجموعات الوظيفية الهيكلية الأساسية مثل alpha- (α- ) أو beta- (β- ) أو gamma- (γ-) أو delta- (δ-) الأحماض الأمينية ؛ تتعلق الفئات الأخرى بالقطبية ، ومستوى الأس الهيدروجيني ، ونوع مجموعة السلسلة الجانبية (الأليفاتية ، أو الحلقية ، أو العطرية ، أو المحتوية على الهيدروكسيل أو الكبريت ، وما إلى ذلك). في شكل بروتينات ، تشكل بقايا الأحماض الأمينية ثاني أكبر مكون (الماء هو الأكبر) في عضلات الإنسان والأنسجة الأخرى. بالإضافة إلى دورها كبقايا في البروتينات ، تشارك الأحماض الأمينية في عدد من العمليات مثل نقل الناقلات العصبية والتخليق الحيوي. |  |
| صيغة أساسها الأحماض الأمينية: التركيبة المعتمدة على الأحماض الأمينية هي نوع من تركيبات حليب الرضع مصنوعة من الأحماض الأمينية الفردية. وهو مضاد للحساسية ومخصص للرضع الذين يعانون من حساسية شديدة للحليب وأمراض معدية معوية مختلفة ، مثل متلازمة التهاب الأمعاء والقولون الناجم عن البروتين الغذائي ومتلازمات سوء الامتصاص. يشار إليها أحيانًا على أنها صيغة عنصرية ولكن هذا يعتبر اسمًا مضللًا. تشمل المشاكل المتعلقة باستخدام الصيغة القائمة على الأحماض الأمينية تكلفتها العالية وطعمها غير المستساغ. لا يظهر تناول تركيبة الأحماض الأمينية للأطفال الأصحاء أي فائدة في النمو. | |
| درجة الأحماض الأمينية: درجة الأحماض الأمينية ، جنبًا إلى جنب مع هضم البروتين ، هي الطريقة المستخدمة لتحديد ما إذا كان البروتين كاملًا. PDCAAS و DIAAS هما المعياران الرئيسيان للبروتين اللذان يحددان اكتمال البروتينات من خلال تركيبها الفريد من الأحماض الأمينية الأساسية. | |
| حمض أميني: الأحماض الأمينية عبارة عن مركبات عضوية تحتوي على مجموعات وظيفية أمينية (–NH 2 ) وكربوكسيل (–COOH) ، جنبًا إلى جنب مع سلسلة جانبية (مجموعة R) خاصة بكل حمض أميني. العناصر الرئيسية للحمض الأميني هي الكربون (C) والهيدروجين (H) والأكسجين (O) والنيتروجين (N) ، على الرغم من وجود عناصر أخرى في السلاسل الجانبية لبعض الأحماض الأمينية. يُعرف حوالي 500 من الأحماض الأمينية التي تحدث بشكل طبيعي اعتبارًا من عام 1983 (على الرغم من ظهور 20 فقط في الشفرة الوراثية) ويمكن تصنيفها بعدة طرق. يمكن تصنيفها وفقًا لمواقع المجموعات الوظيفية الهيكلية الأساسية مثل alpha- (α- ) أو beta- (β- ) أو gamma- (γ-) أو delta- (δ-) الأحماض الأمينية ؛ تتعلق الفئات الأخرى بالقطبية ، ومستوى الأس الهيدروجيني ، ونوع مجموعة السلسلة الجانبية (الأليفاتية ، أو الحلقية ، أو العطرية ، أو المحتوية على الهيدروكسيل أو الكبريت ، وما إلى ذلك). في شكل بروتينات ، تشكل بقايا الأحماض الأمينية ثاني أكبر مكون (الماء هو الأكبر) في عضلات الإنسان والأنسجة الأخرى. بالإضافة إلى دورها كبقايا في البروتينات ، تشارك الأحماض الأمينية في عدد من العمليات مثل نقل الناقلات العصبية والتخليق الحيوي. |  |
| كيكو امينو: Kiku Amino كان مؤلفًا يابانيًا ومترجمًا للأدب الإنجليزي والروسي. حصلت على جائزة أدب المرأة ، وجائزة يوميوري ، وجائزة الأكاديمية اليابانية للفنون. |  |
| محطة أمينو: محطة أمينو هي محطة سكة حديد في Kyōtango ، محافظة كيوتو ، اليابان. |  |
| يوشيهيكو أمينو: يوشيهيكو أمينو كان مؤرخًا ماركسيًا يابانيًا ومفكرًا عامًا ، وربما اشتهر أكثر من غيره بفحصه الجديد للتاريخ الياباني في العصور الوسطى. على الرغم من نشر القليل من أعمال أمينو في الغرب ، إلا أن الكتاب والمؤرخين اليابانيين في اليابان يعتبرون أمينو أحد أهم المؤرخين اليابانيين في القرن العشرين. بعض النتائج التي توصل إليها أمينو متاحة الآن باللغة الإنجليزية ، في سرد حيوي وشخصي للغاية لكيفية قلبه للعديد من الأفكار التقليدية حول التاريخ الياباني. | |
| جليكاين: الجليسين (الرمز Gly أو G ؛) هو حمض أميني يحتوي على ذرة هيدروجين واحدة كسلسلة جانبية. إنه أبسط حمض أميني ثابت (حمض الكرباميك غير مستقر) ، مع الصيغة الكيميائية NH 2 - CH 2 ‐COOH. الجلايسين هو أحد الأحماض الأمينية البروتينية. يتم ترميزه بواسطة جميع الكودونات التي تبدأ بـ GG (GGU ، GGC ، GGA ، GGG). يعتبر الجلايسين جزءًا لا يتجزأ من تكوين حلزونات ألفا في بنية البروتين الثانوية نظرًا لشكله المضغوط. للسبب نفسه ، فهو أكثر الأحماض الأمينية وفرة في الكولاجين الثلاثي الحلزونات. الجليسين هو أيضًا ناقل عصبي مثبط - يمكن أن يتسبب التداخل في إطلاقه داخل الحبل الشوكي (كما يحدث أثناء عدوى المطثية الكزازية ) في حدوث شلل تشنجي بسبب تقلص العضلات غير المقيد. |  |
| أمينو أسيتونيتريل: Aminoacetonitrile هو مركب عضوي مع الصيغة NCCH 2 NH 2 . المركب سائل عديم اللون. إنه غير مستقر في درجة حرارة الغرفة ، بسبب عدم توافق النوكليوفيل الأمين والنتريل الكهربائي. لهذا السبب يتم مواجهتها عادةً على شكل أملاح كلوريد وثنائي كبريتات مشتق الأمونيوم ، أي [NCCH 2 NH 3 ] + Cl - و [NCCH 2 NH 3 ] + HSO 4 - . | |
| حمض أميني: الأحماض الأمينية عبارة عن مركبات عضوية تحتوي على مجموعات وظيفية أمينية (–NH 2 ) وكربوكسيل (–COOH) ، جنبًا إلى جنب مع سلسلة جانبية (مجموعة R) خاصة بكل حمض أميني. العناصر الرئيسية للحمض الأميني هي الكربون (C) والهيدروجين (H) والأكسجين (O) والنيتروجين (N) ، على الرغم من وجود عناصر أخرى في السلاسل الجانبية لبعض الأحماض الأمينية. يُعرف حوالي 500 من الأحماض الأمينية التي تحدث بشكل طبيعي اعتبارًا من عام 1983 (على الرغم من ظهور 20 فقط في الشفرة الوراثية) ويمكن تصنيفها بعدة طرق. يمكن تصنيفها وفقًا لمواقع المجموعات الوظيفية الهيكلية الأساسية مثل alpha- (α- ) أو beta- (β- ) أو gamma- (γ-) أو delta- (δ-) الأحماض الأمينية ؛ تتعلق الفئات الأخرى بالقطبية ، ومستوى الأس الهيدروجيني ، ونوع مجموعة السلسلة الجانبية (الأليفاتية ، أو الحلقية ، أو العطرية ، أو المحتوية على الهيدروكسيل أو الكبريت ، وما إلى ذلك). في شكل بروتينات ، تشكل بقايا الأحماض الأمينية ثاني أكبر مكون (الماء هو الأكبر) في عضلات الإنسان والأنسجة الأخرى. بالإضافة إلى دورها كبقايا في البروتينات ، تشارك الأحماض الأمينية في عدد من العمليات مثل نقل الناقلات العصبية والتخليق الحيوي. |  |
| صيغة أساسها الأحماض الأمينية: التركيبة المعتمدة على الأحماض الأمينية هي نوع من تركيبات حليب الرضع مصنوعة من الأحماض الأمينية الفردية. وهو مضاد للحساسية ومخصص للرضع الذين يعانون من حساسية شديدة للحليب وأمراض معدية معوية مختلفة ، مثل متلازمة التهاب الأمعاء والقولون الناجم عن البروتين الغذائي ومتلازمات سوء الامتصاص. يشار إليها أحيانًا على أنها صيغة عنصرية ولكن هذا يعتبر اسمًا مضللًا. تشمل المشاكل المتعلقة باستخدام الصيغة القائمة على الأحماض الأمينية تكلفتها العالية وطعمها غير المستساغ. لا يظهر تناول تركيبة الأحماض الأمينية للأطفال الأصحاء أي فائدة في النمو. | |
| نيتروجين الخميرة: نيتروجين الخميرة أو YAN هو مزيج من النيتروجين الأميني الحر (FAN) والأمونيا (NH 3 ) والأمونيوم (NH 4 + ) المتاح لخميرة النبيذ Saccharomyces cerevisiae لاستخدامه أثناء التخمير. بعيدًا عن السكريات القابلة للتخمير ، الجلوكوز والفركتوز ، يعد النيتروجين أهم العناصر الغذائية اللازمة لإجراء عملية تخمير ناجحة لا تنتهي قبل نقطة الجفاف المقصودة أو تشهد تطور الروائح الكريهة وأعطال النبيذ ذات الصلة. إلى هذا الحد ، غالبًا ما يكمل صانعو النبيذ موارد YAN المتاحة بإضافات النيتروجين مثل فوسفات ثنائي الأمونيوم (DAP). |  |
| ليسين: Lysine (رمز Lys أو K ) هو حمض أميني ألفا يستخدم في التخليق الحيوي للبروتينات. يحتوي على مجموعة α-amino (الموجودة في شكل −NH 3 + البروتوني تحت الظروف البيولوجية) ، ومجموعة حمض α-carboxylic (الموجودة في شكل −COO - في ظل الظروف البيولوجية) ، وسلسلة جانبية ليسيل ( (CH 2 ) 4 NH 2 ) ، ويصنفه على أنه حمض أميني أليفاتي أساسي ، مشحون (عند درجة الحموضة الفسيولوجية). يتم ترميزه بواسطة كودونات AAA و AAG. مثل جميع الأحماض الأمينية الأخرى تقريبًا ، فإن α-carbon يكون مراوانًا وقد يشير اللايسين إلى إما متماثل أو خليط راسيمي من كليهما. لغرض هذه المقالة ، سوف يشير اللايسين إلى المتشاهد النشط بيولوجيًا L-lysine ، حيث يكون α-carbon في التكوين S. | 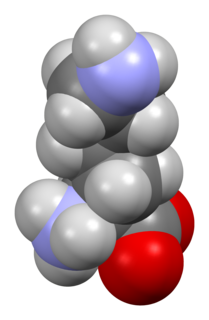 |
| الهليون: الأسباراجين هو حمض أميني ألفا يستخدم في التخليق الحيوي للبروتينات. يحتوي على مجموعة α-amino ، ومجموعة حمض α-carboxylic ، وسلسلة جانبية كربوكساميد ، ويصنفها على أنها حمض أميني قطبي أليفاتي. إنه غير ضروري للبشر ، مما يعني أن الجسم يمكنه تصنيعه. يتم ترميزه بواسطة الكودونات AAU و AAC. | 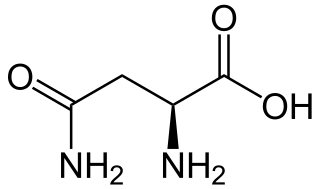 |
| الأحماض الأمينية N-carboxyanhydride: الأحماض الأمينية N- carboxyanhydrides ، وتسمى أيضًا أنهيدريد Leuchs ، هي مشتقات تفاعلية من الأحماض الأمينية. يتم استخدامها في مجال المواد الحيوية لتطبيقاتها في توصيل الأدوية والعلاج الجيني والمضادات الحيوية وهندسة الأنسجة. عادة ، يتم اشتقاق هذه المركبات من الأحماض الأمينية عن طريق المعالجة بـ triphosgene ، و phosgene ، و PCl 5 ، وكواشف الهالوجين الأخرى. يمكن استخدام NCAs لإعداد البولي ببتيدات من خلال بلمرة فتح الحلقة ، وهو نهج عملي لإنتاج البولي ببتيدات على نطاق واسع حيث تكون خصوصية التسلسل أقل أهمية من الخصائص الفيزيائية السائبة. تجد هذه المركبات تطبيقًا في الكيمياء الحيوية والهندسة الطبية الحيوية وتكنولوجيا النانو نظرًا لميلها إلى البلمرة عند المعالجة بالنيوكليوفيل ، هيكساميثيلديسيلازان ، ومعادن انتقالية لإنشاء بولي ببتيدات. تشير الدلائل إلى أن هذه المركبات قد تكون متورطة في التولد الذاتي. | |
| حمض أميني: الأحماض الأمينية عبارة عن مركبات عضوية تحتوي على مجموعات وظيفية أمينية (–NH 2 ) وكربوكسيل (–COOH) ، جنبًا إلى جنب مع سلسلة جانبية (مجموعة R) خاصة بكل حمض أميني. العناصر الرئيسية للحمض الأميني هي الكربون (C) والهيدروجين (H) والأكسجين (O) والنيتروجين (N) ، على الرغم من وجود عناصر أخرى في السلاسل الجانبية لبعض الأحماض الأمينية. يُعرف حوالي 500 من الأحماض الأمينية التي تحدث بشكل طبيعي اعتبارًا من عام 1983 (على الرغم من ظهور 20 فقط في الشفرة الوراثية) ويمكن تصنيفها بعدة طرق. يمكن تصنيفها وفقًا لمواقع المجموعات الوظيفية الهيكلية الأساسية مثل alpha- (α- ) أو beta- (β- ) أو gamma- (γ-) أو delta- (δ-) الأحماض الأمينية ؛ تتعلق الفئات الأخرى بالقطبية ، ومستوى الأس الهيدروجيني ، ونوع مجموعة السلسلة الجانبية (الأليفاتية ، أو الحلقية ، أو العطرية ، أو المحتوية على الهيدروكسيل أو الكبريت ، وما إلى ذلك). في شكل بروتينات ، تشكل بقايا الأحماض الأمينية ثاني أكبر مكون (الماء هو الأكبر) في عضلات الإنسان والأنسجة الأخرى. بالإضافة إلى دورها كبقايا في البروتينات ، تشارك الأحماض الأمينية في عدد من العمليات مثل نقل الناقلات العصبية والتخليق الحيوي. |  |
| تنشيط الأحماض الأمينية: يشير تنشيط الأحماض الأمينية إلى ارتباط الحمض الأميني بنقل الحمض النووي الريبي (الحمض الريبي النووي النقال).
| |
| حمض أميني: الأحماض الأمينية عبارة عن مركبات عضوية تحتوي على مجموعات وظيفية أمينية (–NH 2 ) وكربوكسيل (–COOH) ، جنبًا إلى جنب مع سلسلة جانبية (مجموعة R) خاصة بكل حمض أميني. العناصر الرئيسية للحمض الأميني هي الكربون (C) والهيدروجين (H) والأكسجين (O) والنيتروجين (N) ، على الرغم من وجود عناصر أخرى في السلاسل الجانبية لبعض الأحماض الأمينية. يُعرف حوالي 500 من الأحماض الأمينية التي تحدث بشكل طبيعي اعتبارًا من عام 1983 (على الرغم من ظهور 20 فقط في الشفرة الوراثية) ويمكن تصنيفها بعدة طرق. يمكن تصنيفها وفقًا لمواقع المجموعات الوظيفية الهيكلية الأساسية مثل alpha- (α- ) أو beta- (β- ) أو gamma- (γ-) أو delta- (δ-) الأحماض الأمينية ؛ تتعلق الفئات الأخرى بالقطبية ، ومستوى الأس الهيدروجيني ، ونوع مجموعة السلسلة الجانبية (الأليفاتية ، أو الحلقية ، أو العطرية ، أو المحتوية على الهيدروكسيل أو الكبريت ، وما إلى ذلك). في شكل بروتينات ، تشكل بقايا الأحماض الأمينية ثاني أكبر مكون (الماء هو الأكبر) في عضلات الإنسان والأنسجة الأخرى. بالإضافة إلى دورها كبقايا في البروتينات ، تشارك الأحماض الأمينية في عدد من العمليات مثل نقل الناقلات العصبية والتخليق الحيوي. |  |
| حمض أميني: الأحماض الأمينية عبارة عن مركبات عضوية تحتوي على مجموعات وظيفية أمينية (–NH 2 ) وكربوكسيل (–COOH) ، جنبًا إلى جنب مع سلسلة جانبية (مجموعة R) خاصة بكل حمض أميني. العناصر الرئيسية للحمض الأميني هي الكربون (C) والهيدروجين (H) والأكسجين (O) والنيتروجين (N) ، على الرغم من وجود عناصر أخرى في السلاسل الجانبية لبعض الأحماض الأمينية. يُعرف حوالي 500 من الأحماض الأمينية التي تحدث بشكل طبيعي اعتبارًا من عام 1983 (على الرغم من ظهور 20 فقط في الشفرة الوراثية) ويمكن تصنيفها بعدة طرق. يمكن تصنيفها وفقًا لمواقع المجموعات الوظيفية الهيكلية الأساسية مثل alpha- (α- ) أو beta- (β- ) أو gamma- (γ-) أو delta- (δ-) الأحماض الأمينية ؛ تتعلق الفئات الأخرى بالقطبية ، ومستوى الأس الهيدروجيني ، ونوع مجموعة السلسلة الجانبية (الأليفاتية ، أو الحلقية ، أو العطرية ، أو المحتوية على الهيدروكسيل أو الكبريت ، وما إلى ذلك). في شكل بروتينات ، تشكل بقايا الأحماض الأمينية ثاني أكبر مكون (الماء هو الأكبر) في عضلات الإنسان والأنسجة الأخرى. بالإضافة إلى دورها كبقايا في البروتينات ، تشارك الأحماض الأمينية في عدد من العمليات مثل نقل الناقلات العصبية والتخليق الحيوي. |  |
| حمض أميني: الأحماض الأمينية عبارة عن مركبات عضوية تحتوي على مجموعات وظيفية أمينية (–NH 2 ) وكربوكسيل (–COOH) ، جنبًا إلى جنب مع سلسلة جانبية (مجموعة R) خاصة بكل حمض أميني. العناصر الرئيسية للحمض الأميني هي الكربون (C) والهيدروجين (H) والأكسجين (O) والنيتروجين (N) ، على الرغم من وجود عناصر أخرى في السلاسل الجانبية لبعض الأحماض الأمينية. يُعرف حوالي 500 من الأحماض الأمينية التي تحدث بشكل طبيعي اعتبارًا من عام 1983 (على الرغم من ظهور 20 فقط في الشفرة الوراثية) ويمكن تصنيفها بعدة طرق. يمكن تصنيفها وفقًا لمواقع المجموعات الوظيفية الهيكلية الأساسية مثل alpha- (α- ) أو beta- (β- ) أو gamma- (γ-) أو delta- (δ-) الأحماض الأمينية ؛ تتعلق الفئات الأخرى بالقطبية ، ومستوى الأس الهيدروجيني ، ونوع مجموعة السلسلة الجانبية (الأليفاتية ، أو الحلقية ، أو العطرية ، أو المحتوية على الهيدروكسيل أو الكبريت ، وما إلى ذلك). في شكل بروتينات ، تشكل بقايا الأحماض الأمينية ثاني أكبر مكون (الماء هو الأكبر) في عضلات الإنسان والأنسجة الأخرى. بالإضافة إلى دورها كبقايا في البروتينات ، تشارك الأحماض الأمينية في عدد من العمليات مثل نقل الناقلات العصبية والتخليق الحيوي. |  |
| تسلسل البروتين: تسلسل البروتين هو العملية العملية لتحديد تسلسل الأحماض الأمينية لكل أو جزء من البروتين أو الببتيد. قد يعمل هذا على تحديد البروتين أو وصف تعديلاته اللاحقة للترجمة. عادةً ما يوفر التسلسل الجزئي للبروتين معلومات كافية لتحديده بالرجوع إلى قواعد بيانات تسلسلات البروتين المشتقة من الترجمة المفاهيمية للجينات. |  |
| Autoradiograph: وصورة الإشعاع الذاتي هو صورة على فيلم الأشعة السينية أو مستحلب النووي التي تنتجها نمط من انبعاثات تسوس من توزيع مادة مشعة. بدلاً من ذلك ، يتوفر جهاز التصوير الشعاعي الذاتي أيضًا كصورة رقمية ، نظرًا للتطور الأخير لكاشفات غاز التلألؤ أو أنظمة تصوير الفسفور الأرضي النادرة. يتم وضع الفيلم أو المستحلب على قسم الأنسجة المسمى للحصول على صورة الأشعة. تشير البادئة التلقائية إلى أن المادة المشعة موجودة داخل العينة ، على عكس حالة التأريخ الإشعاعي أو التصوير الشعاعي الدقيق ، حيث يتم تمييز العينة باستخدام مصدر خارجي. يمكن فحص بعض الصور الشعاعية الذاتية مجهريًا لتحديد موقع حبيبات الفضة التي تسمى العملية تصوير الإشعاع الذاتي الدقيق. على سبيل المثال ، تم استخدام التصوير الإشعاعي الذاتي الدقيق لفحص ما إذا كان الأترازين يتم استقلابه بواسطة نبات نباتات زهقرنية أو عن طريق الكائنات الحية الدقيقة المشبعة في طبقة الأغشية الحيوية المحيطة بالنبات. |  |
| صيغة أساسها الأحماض الأمينية: التركيبة المعتمدة على الأحماض الأمينية هي نوع من تركيبات حليب الرضع مصنوعة من الأحماض الأمينية الفردية. وهو مضاد للحساسية ومخصص للرضع الذين يعانون من حساسية شديدة للحليب وأمراض معدية معوية مختلفة ، مثل متلازمة التهاب الأمعاء والقولون الناجم عن البروتين الغذائي ومتلازمات سوء الامتصاص. يشار إليها أحيانًا على أنها صيغة عنصرية ولكن هذا يعتبر اسمًا مضللًا. تشمل المشاكل المتعلقة باستخدام الصيغة القائمة على الأحماض الأمينية تكلفتها العالية وطعمها غير المستساغ. لا يظهر تناول تركيبة الأحماض الأمينية للأطفال الأصحاء أي فائدة في النمو. | |
| حمض أميني: الأحماض الأمينية عبارة عن مركبات عضوية تحتوي على مجموعات وظيفية أمينية (–NH 2 ) وكربوكسيل (–COOH) ، جنبًا إلى جنب مع سلسلة جانبية (مجموعة R) خاصة بكل حمض أميني. العناصر الرئيسية للحمض الأميني هي الكربون (C) والهيدروجين (H) والأكسجين (O) والنيتروجين (N) ، على الرغم من وجود عناصر أخرى في السلاسل الجانبية لبعض الأحماض الأمينية. يُعرف حوالي 500 من الأحماض الأمينية التي تحدث بشكل طبيعي اعتبارًا من عام 1983 (على الرغم من ظهور 20 فقط في الشفرة الوراثية) ويمكن تصنيفها بعدة طرق. يمكن تصنيفها وفقًا لمواقع المجموعات الوظيفية الهيكلية الأساسية مثل alpha- (α- ) أو beta- (β- ) أو gamma- (γ-) أو delta- (δ-) الأحماض الأمينية ؛ تتعلق الفئات الأخرى بالقطبية ، ومستوى الأس الهيدروجيني ، ونوع مجموعة السلسلة الجانبية (الأليفاتية ، أو الحلقية ، أو العطرية ، أو المحتوية على الهيدروكسيل أو الكبريت ، وما إلى ذلك). في شكل بروتينات ، تشكل بقايا الأحماض الأمينية ثاني أكبر مكون (الماء هو الأكبر) في عضلات الإنسان والأنسجة الأخرى. بالإضافة إلى دورها كبقايا في البروتينات ، تشارك الأحماض الأمينية في عدد من العمليات مثل نقل الناقلات العصبية والتخليق الحيوي. |  |
| حمض أميني: الأحماض الأمينية عبارة عن مركبات عضوية تحتوي على مجموعات وظيفية أمينية (–NH 2 ) وكربوكسيل (–COOH) ، جنبًا إلى جنب مع سلسلة جانبية (مجموعة R) خاصة بكل حمض أميني. العناصر الرئيسية للحمض الأميني هي الكربون (C) والهيدروجين (H) والأكسجين (O) والنيتروجين (N) ، على الرغم من وجود عناصر أخرى في السلاسل الجانبية لبعض الأحماض الأمينية. يُعرف حوالي 500 من الأحماض الأمينية التي تحدث بشكل طبيعي اعتبارًا من عام 1983 (على الرغم من ظهور 20 فقط في الشفرة الوراثية) ويمكن تصنيفها بعدة طرق. يمكن تصنيفها وفقًا لمواقع المجموعات الوظيفية الهيكلية الأساسية مثل alpha- (α- ) أو beta- (β- ) أو gamma- (γ-) أو delta- (δ-) الأحماض الأمينية ؛ تتعلق الفئات الأخرى بالقطبية ، ومستوى الأس الهيدروجيني ، ونوع مجموعة السلسلة الجانبية (الأليفاتية ، أو الحلقية ، أو العطرية ، أو المحتوية على الهيدروكسيل أو الكبريت ، وما إلى ذلك). في شكل بروتينات ، تشكل بقايا الأحماض الأمينية ثاني أكبر مكون (الماء هو الأكبر) في عضلات الإنسان والأنسجة الأخرى. بالإضافة إلى دورها كبقايا في البروتينات ، تشارك الأحماض الأمينية في عدد من العمليات مثل نقل الناقلات العصبية والتخليق الحيوي. |  |
| حمض أميني: الأحماض الأمينية عبارة عن مركبات عضوية تحتوي على مجموعات وظيفية أمينية (–NH 2 ) وكربوكسيل (–COOH) ، جنبًا إلى جنب مع سلسلة جانبية (مجموعة R) خاصة بكل حمض أميني. العناصر الرئيسية للحمض الأميني هي الكربون (C) والهيدروجين (H) والأكسجين (O) والنيتروجين (N) ، على الرغم من وجود عناصر أخرى في السلاسل الجانبية لبعض الأحماض الأمينية. يُعرف حوالي 500 من الأحماض الأمينية التي تحدث بشكل طبيعي اعتبارًا من عام 1983 (على الرغم من ظهور 20 فقط في الشفرة الوراثية) ويمكن تصنيفها بعدة طرق. يمكن تصنيفها وفقًا لمواقع المجموعات الوظيفية الهيكلية الأساسية مثل alpha- (α- ) أو beta- (β- ) أو gamma- (γ-) أو delta- (δ-) الأحماض الأمينية ؛ تتعلق الفئات الأخرى بالقطبية ، ومستوى الأس الهيدروجيني ، ونوع مجموعة السلسلة الجانبية (الأليفاتية ، أو الحلقية ، أو العطرية ، أو المحتوية على الهيدروكسيل أو الكبريت ، وما إلى ذلك). في شكل بروتينات ، تشكل بقايا الأحماض الأمينية ثاني أكبر مكون (الماء هو الأكبر) في عضلات الإنسان والأنسجة الأخرى. بالإضافة إلى دورها كبقايا في البروتينات ، تشارك الأحماض الأمينية في عدد من العمليات مثل نقل الناقلات العصبية والتخليق الحيوي. |  |
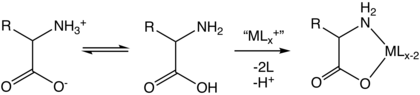
| مجمعات الأحماض الأمينية المعدنية الانتقالية: مجمعات الأحماض الأمينية المعدنية الانتقالية هي عائلة كبيرة من مجمعات التنسيق التي تحتوي على القواعد المترافقة للأحماض الأمينية ، 2-aminocarboxylates. الأحماض الأمينية منتشرة في الطبيعة ، وكلها تعمل كروابط نحو المعادن الانتقالية. لا تشتمل هذه المقالة على مجمعات من مشتقات الأميدات والإستر للأحماض الأمينية. كما تم استبعاد أحماض البولي أمينو بما في ذلك العوامل المخلبية EDTA و NTA. | |
| تأريخ الأحماض الأمينية: التأريخ بالأحماض الأمينية هو تقنية تأريخ تستخدم لتقدير عمر عينة في علم الأحياء القديمة ، وعلم الحفريات الجزيئي ، وعلم الآثار ، وعلم الطب الشرعي ، وعلم الطب ، والجيولوجيا الرسوبية وغيرها من المجالات. تربط هذه التقنية التغييرات في جزيئات الأحماض الأمينية بالوقت المنقضي منذ تشكلها. | |
| ديكاربوكسيلاز الأحماض الأمينية العطرية: كربوكسيل حمض العطرية L -amino، المعروف أيضا باسم دوبا كربوكسيل (DDC)، التربتوفان كربوكسيل، و5-هيدروكسيتريبتوفان كربوكسيل، هو ياز الانزيم. |  |
| حمض أميني: الأحماض الأمينية عبارة عن مركبات عضوية تحتوي على مجموعات وظيفية أمينية (–NH 2 ) وكربوكسيل (–COOH) ، جنبًا إلى جنب مع سلسلة جانبية (مجموعة R) خاصة بكل حمض أميني. العناصر الرئيسية للحمض الأميني هي الكربون (C) والهيدروجين (H) والأكسجين (O) والنيتروجين (N) ، على الرغم من وجود عناصر أخرى في السلاسل الجانبية لبعض الأحماض الأمينية. يُعرف حوالي 500 من الأحماض الأمينية التي تحدث بشكل طبيعي اعتبارًا من عام 1983 (على الرغم من ظهور 20 فقط في الشفرة الوراثية) ويمكن تصنيفها بعدة طرق. يمكن تصنيفها وفقًا لمواقع المجموعات الوظيفية الهيكلية الأساسية مثل alpha- (α- ) أو beta- (β- ) أو gamma- (γ-) أو delta- (δ-) الأحماض الأمينية ؛ تتعلق الفئات الأخرى بالقطبية ، ومستوى الأس الهيدروجيني ، ونوع مجموعة السلسلة الجانبية (الأليفاتية ، أو الحلقية ، أو العطرية ، أو المحتوية على الهيدروكسيل أو الكبريت ، وما إلى ذلك). في شكل بروتينات ، تشكل بقايا الأحماض الأمينية ثاني أكبر مكون (الماء هو الأكبر) في عضلات الإنسان والأنسجة الأخرى. بالإضافة إلى دورها كبقايا في البروتينات ، تشارك الأحماض الأمينية في عدد من العمليات مثل نقل الناقلات العصبية والتخليق الحيوي. |  |
| كيناز الأحماض الأمينية: في البيولوجيا الجزيئية ، مجال كيناز الأحماض الأمينية هو مجال بروتيني. يوجد في كينازات البروتين بخصائص مختلفة ، بما في ذلك عائلات الأسبارتات والغلوتامات ويوريديليت كيناز. في بدائيات النوى والنباتات ، يتم تنظيم تخليق الأحماض الأمينية الأساسية ليسين وثريونين في الغالب عن طريق تثبيط التغذية المرتدة لأسبارتات كيناز (AK) وسينثاز ثنائي هيدروديبيكولين (DHPS). في Escherichia coli ، تُشفِّر ثرA و metLM و lysC إنزيمات الأسبارتوكيناز التي تُظهر تثبيطًا للتغذية الراجعة بواسطة ثريونين وميثيونين ولايسين ، على التوالي. يحتوي الإنزيم المتماثل الحساس لليسين لأسبارتات كيناز من أوراق السبانخ على تكوين وحدة فرعية من 4 وحدات فرعية كبيرة و 4 وحدات فرعية صغيرة. |  |
| استقلاب البروتين: يشير التمثيل الغذائي للبروتين إلى العمليات الكيميائية الحيوية المختلفة المسؤولة عن تخليق البروتينات والأحماض الأمينية ( التمثيل الغذائي ) ، وتفكك البروتينات عن طريق الهدم. | |
| الحافز الإنشائي: في جزيء بيولوجي شبيه بالسلسلة ، مثل البروتين أو الحمض النووي ، يكون الحافز البنيوي عبارة عن بنية ثلاثية الأبعاد شائعة تظهر في مجموعة متنوعة من الجزيئات المختلفة غير المرتبطة تطوريًا. لا يجب أن يرتبط التصميم الهيكلي بعنصر تسلسلي ؛ يمكن تمثيله بتسلسلات مختلفة وغير مرتبطة تمامًا في بروتينات مختلفة أو RNA. | |
| الناقل العصبي للأحماض الأمينية: الناقل العصبي للأحماض الأمينية هو حمض أميني قادر على نقل رسالة عصبية عبر المشبك. يتم حزم الناقلات العصبية (المواد الكيميائية) في حويصلات تتجمع تحت الغشاء الطرفي للمحور على الجانب قبل المشبكي من المشبك في عملية تسمى الالتقام الخلوي. |  |
| حمض أميني: الأحماض الأمينية عبارة عن مركبات عضوية تحتوي على مجموعات وظيفية أمينية (–NH 2 ) وكربوكسيل (–COOH) ، جنبًا إلى جنب مع سلسلة جانبية (مجموعة R) خاصة بكل حمض أميني. العناصر الرئيسية للحمض الأميني هي الكربون (C) والهيدروجين (H) والأكسجين (O) والنيتروجين (N) ، على الرغم من وجود عناصر أخرى في السلاسل الجانبية لبعض الأحماض الأمينية. يُعرف حوالي 500 من الأحماض الأمينية التي تحدث بشكل طبيعي اعتبارًا من عام 1983 (على الرغم من ظهور 20 فقط في الشفرة الوراثية) ويمكن تصنيفها بعدة طرق. يمكن تصنيفها وفقًا لمواقع المجموعات الوظيفية الهيكلية الأساسية مثل alpha- (α- ) أو beta- (β- ) أو gamma- (γ-) أو delta- (δ-) الأحماض الأمينية ؛ تتعلق الفئات الأخرى بالقطبية ، ومستوى الأس الهيدروجيني ، ونوع مجموعة السلسلة الجانبية (الأليفاتية ، أو الحلقية ، أو العطرية ، أو المحتوية على الهيدروكسيل أو الكبريت ، وما إلى ذلك). في شكل بروتينات ، تشكل بقايا الأحماض الأمينية ثاني أكبر مكون (الماء هو الأكبر) في عضلات الإنسان والأنسجة الأخرى. بالإضافة إلى دورها كبقايا في البروتينات ، تشارك الأحماض الأمينية في عدد من العمليات مثل نقل الناقلات العصبية والتخليق الحيوي. |  |
| أكسدة حامض أميني: إن أوكسيدوروكتازات الأحماض الأمينية هي نوع من الإنزيمات المؤكسدة التي تعمل على الأحماض الأمينية. | |
| نفاذية الأحماض الأمينية: تصاريح الأحماض الأمينية هي تراخيص غشاء تشارك في نقل الأحماض الأمينية إلى الخلية تم العثور على عدد من هذه البروتينات لتكون ذات صلة تطورية. تحتوي هذه البروتينات على 12 قطعة غشائية. | |
| الأحماض الأمينية الأساسية: الحمض الأميني الأساسي ، أو الأحماض الأمينية التي لا غنى عنها ، هو حمض أميني لا يمكن للكائن تصنيعه من الصفر بسرعة كافية لتلبية احتياجاته ، وبالتالي يجب أن يأتي من النظام الغذائي. من بين الأحماض الأمينية الـ 21 الشائعة في جميع أشكال الحياة ، فإن الأحماض الأمينية التسعة التي لا يستطيع البشر تصنيعها هي فينيل ألانين ، فالين ، ثريونين ، تريبتوفان ، ميثيونين ، ليوسين ، إيزولوسين ، ليسين ، وهستيدين. | |
| استبدال الأحماض الأمينية: استبدال الأحماض الأمينية هو تغيير من حمض أميني واحد إلى حمض أميني مختلف في البروتين بسبب طفرة نقطية في تسلسل الحمض النووي المقابل. وهو ناتج عن طفرة خاطئة غير معروفة والتي تغير تسلسل الكودون لتشفير حمض أميني آخر بدلاً من الأصل. | |
| هيكل البروتين: بنية البروتين هي الترتيب ثلاثي الأبعاد للذرات في جزيء سلسلة الأحماض الأمينية. البروتينات عبارة عن بوليمرات - خاصة عديد الببتيدات - تتكون من متواليات من الأحماض الأمينية ، مونومرات البوليمر. يمكن أيضًا تسمية مونومر حمض أميني واحد ببقايا تشير إلى وحدة متكررة من البوليمر. تتكون البروتينات من الأحماض الأمينية التي تخضع لتفاعلات التكثيف ، حيث تفقد الأحماض الأمينية جزيء ماء واحدًا لكل تفاعل من أجل الارتباط ببعضها البعض برابطة الببتيد. وفقًا للاتفاقية ، غالبًا ما يتم تحديد سلسلة تحت 30 من الأحماض الأمينية على أنها ببتيد ، وليس بروتين. لتكون قادرة على أداء وظيفتها البيولوجية ، يتم طي البروتينات في واحد أو أكثر من التوافق المكاني المحدد مدفوعًا بعدد من التفاعلات غير التساهمية مثل الترابط الهيدروجيني ، والتفاعلات الأيونية ، وقوى فان دير فال ، والتعبئة الكارهة للماء. لفهم وظائف البروتينات على المستوى الجزيئي ، غالبًا ما يكون من الضروري تحديد هيكلها ثلاثي الأبعاد. هذا هو موضوع المجال العلمي للبيولوجيا الهيكلية ، والذي يستخدم تقنيات مثل علم البلورات بالأشعة السينية ، والتحليل الطيفي بالرنين المغناطيسي النووي ، والمجهر الإلكتروني بالتبريد (cryo-EM) وقياس التداخل ثنائي الاستقطاب لتحديد بنية البروتينات. |  |
| هيكل البروتين: بنية البروتين هي الترتيب ثلاثي الأبعاد للذرات في جزيء سلسلة الأحماض الأمينية. البروتينات عبارة عن بوليمرات - خاصة عديد الببتيدات - تتكون من متواليات من الأحماض الأمينية ، مونومرات البوليمر. يمكن أيضًا تسمية مونومر حمض أميني واحد ببقايا تشير إلى وحدة متكررة من البوليمر. تتكون البروتينات من الأحماض الأمينية التي تخضع لتفاعلات التكثيف ، حيث تفقد الأحماض الأمينية جزيء ماء واحدًا لكل تفاعل من أجل الارتباط ببعضها البعض برابطة الببتيد. وفقًا للاتفاقية ، غالبًا ما يتم تحديد سلسلة تحت 30 من الأحماض الأمينية على أنها ببتيد ، وليس بروتين. لتكون قادرة على أداء وظيفتها البيولوجية ، يتم طي البروتينات في واحد أو أكثر من التوافق المكاني المحدد مدفوعًا بعدد من التفاعلات غير التساهمية مثل الترابط الهيدروجيني ، والتفاعلات الأيونية ، وقوى فان دير فال ، والتعبئة الكارهة للماء. لفهم وظائف البروتينات على المستوى الجزيئي ، غالبًا ما يكون من الضروري تحديد هيكلها ثلاثي الأبعاد. هذا هو موضوع المجال العلمي للبيولوجيا الهيكلية ، والذي يستخدم تقنيات مثل علم البلورات بالأشعة السينية ، والتحليل الطيفي بالرنين المغناطيسي النووي ، والمجهر الإلكتروني بالتبريد (cryo-EM) وقياس التداخل ثنائي الاستقطاب لتحديد بنية البروتينات. |  |
| استجابة الأحماض الأمينية: استجابة الأحماض الأمينية هي الآلية التي يتم تشغيلها في خلايا الثدييات عن طريق تجويع الأحماض الأمينية. | |
| مثبطات امتصاص الأحماض الأمينية: مثبطات امتصاص الأحماض الأمينية ( AARI ) هي نوع من الأدوية التي تمنع إعادة امتصاص واحد أو أكثر من الناقلات العصبية للأحماض الأمينية عن طريق منع واحد أو أكثر من ناقلات كل منها. وهي تشمل مثبطات امتصاص الأحماض الأمينية المثيرة ، ومثبطات امتصاص GABA ، ومثبطات امتصاص الجلايسين. | |
| درجة الأحماض الأمينية: درجة الأحماض الأمينية ، جنبًا إلى جنب مع هضم البروتين ، هي الطريقة المستخدمة لتحديد ما إذا كان البروتين كاملًا. PDCAAS و DIAAS هما المعياران الرئيسيان للبروتين اللذان يحددان اكتمال البروتينات من خلال تركيبها الفريد من الأحماض الأمينية الأساسية. | |
| الهيكل الأساسي للبروتين: التركيب الأساسي للبروتين هو التسلسل الخطي للأحماض الأمينية في الببتيد أو البروتين. وفقًا للاتفاقية ، يتم الإبلاغ عن الهيكل الأساسي للبروتين بدءًا من الطرف الأميني (N) إلى نهاية الطرف الكربوكسيل (C). يتم إجراء التخليق الحيوي للبروتين بشكل شائع بواسطة الريبوسومات في الخلايا. يمكن أيضًا تصنيع الببتيدات في المختبر. يمكن تسلسل الهياكل الأولية للبروتين مباشرة ، أو استنتاجها من تسلسل الحمض النووي. |  |
| تجانس التسلسل: تماثل التسلسل هو التناظر البيولوجي بين تسلسل الحمض النووي أو الحمض النووي الريبي أو البروتين ، المحدد من حيث الأصل المشترك في التاريخ التطوري للحياة. يمكن أن يكون لقطعتين من الحمض النووي سلالة مشتركة بسبب ثلاث ظواهر: إما حدث انتواع (تقويم العظام) ، أو حدث ازدواجية (نظراء) ، أو حدث نقل جيني أفقي (xenologs). | 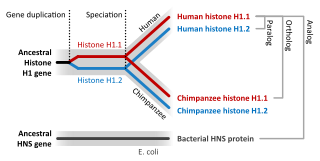 |
| تخليق الأحماض الأمينية: تخليق الأحماض الأمينية هو مجموعة العمليات الكيميائية الحيوية التي يتم من خلالها إنتاج الأحماض الأمينية. ركائز هذه العمليات هي مركبات مختلفة في النظام الغذائي للكائن الحي أو وسط النمو. ليست كل الكائنات الحية قادرة على تصنيع جميع الأحماض الأمينية. على سبيل المثال ، يمكن للبشر فقط تصنيع 11 من أصل 20 حمضًا أمينيًا قياسيًا ، وفي وقت النمو المتسارع ، يمكن اعتبار الهيستدين حمض أميني أساسي. |  |
| اضطراب نقل الأحماض الأمينية: اضطرابات نقل الأحماض الأمينية هي حالات طبية مرتبطة بفشل الأحماض الأمينية ليتم امتصاصها من الكلى أو الأمعاء. | |
| اضطراب نقل الأحماض الأمينية: اضطرابات نقل الأحماض الأمينية هي حالات طبية مرتبطة بفشل الأحماض الأمينية ليتم امتصاصها من الكلى أو الأمعاء. | |
| ناقل الغلوتامات: ناقلات الغلوتامات هي عائلة من البروتينات الناقلة للناقلات العصبية التي تنقل الغلوتامات - الناقل العصبي الرئيسي المثير - عبر الغشاء. تتكون عائلة ناقلات الغلوتامات من فئتين فرعيتين أساسيتين: عائلة ناقل الأحماض الأمينية المثيرة ( EAAT ) وعائلة ناقل الغلوتامات الحويصلي ( VGLUT ). في الدماغ ، تقوم EAAT بإزالة الغلوتامات من الشق المشبكي والمواقع خارج المشبكية عن طريق إعادة امتصاص الغلوتامات في الخلايا الدبقية والخلايا العصبية ، بينما تقوم VGLUTs بنقل الغلوتامات من سيتوبلازم الخلية إلى حويصلات متشابكة. تقوم ناقلات الجلوتامات أيضًا بنقل الأسبارتات وهي موجودة فعليًا في جميع الأنسجة المحيطية ، بما في ذلك القلب والكبد والخصيتين والعظام. إنها تظهر الانتقائية الفراغية لـ L-glutamate ولكنها تنقل كل من L-aspartate و D-aspartate. | |
| بروتين النقل: بروتين النقل هو بروتين يقوم بوظيفة نقل المواد الأخرى داخل الكائن الحي. تعتبر بروتينات النقل حيوية لنمو وحياة جميع الكائنات الحية. هناك عدة أنواع مختلفة من بروتينات النقل. |  |
| حامض: الحمض عبارة عن جزيء أو أيون قادر على التبرع بالبروتون (أي ، أيون الهيدروجين ، H + ) ، المعروف باسم حمض Brønsted – Lowry ، أو قادر على تكوين رابطة تساهمية مع زوج إلكترون ، يُعرف باسم حمض لويس. |  |
| قاعدة (كيمياء): في الكيمياء ، هناك ثلاثة تعريفات شائعة الاستخدام لكلمة قاعدة ، والمعروفة باسم قواعد أرهينيوس ، وقواعد برونستيد ، وقواعد لويس. تتفق جميع التعاريف على أن القواعد هي مواد تتفاعل مع الأحماض كما اقترح في الأصل G.-F. Rouelle في منتصف القرن الثامن عشر. |  |
| بروتين النقل: بروتين النقل هو بروتين يقوم بوظيفة نقل المواد الأخرى داخل الكائن الحي. تعتبر بروتينات النقل حيوية لنمو وحياة جميع الكائنات الحية. هناك عدة أنواع مختلفة من بروتينات النقل. |  |
| ناقل الأحماض الأمينية: ناقل الأحماض الأمينية هو بروتين نقل غشاء ينقل الأحماض الأمينية. هم أساسا من عائلة الناقل المذاب. | |
| مثبطات امتصاص الأحماض الأمينية: مثبطات امتصاص الأحماض الأمينية ( AARI ) هي نوع من الأدوية التي تمنع إعادة امتصاص واحد أو أكثر من الناقلات العصبية للأحماض الأمينية عن طريق منع واحد أو أكثر من ناقلات كل منها. وهي تشمل مثبطات امتصاص الأحماض الأمينية المثيرة ، ومثبطات امتصاص GABA ، ومثبطات امتصاص الجلايسين. | |
| حمض أميني: الأحماض الأمينية عبارة عن مركبات عضوية تحتوي على مجموعات وظيفية أمينية (–NH 2 ) وكربوكسيل (–COOH) ، جنبًا إلى جنب مع سلسلة جانبية (مجموعة R) خاصة بكل حمض أميني. العناصر الرئيسية للحمض الأميني هي الكربون (C) والهيدروجين (H) والأكسجين (O) والنيتروجين (N) ، على الرغم من وجود عناصر أخرى في السلاسل الجانبية لبعض الأحماض الأمينية. يُعرف حوالي 500 من الأحماض الأمينية التي تحدث بشكل طبيعي اعتبارًا من عام 1983 (على الرغم من ظهور 20 فقط في الشفرة الوراثية) ويمكن تصنيفها بعدة طرق. يمكن تصنيفها وفقًا لمواقع المجموعات الوظيفية الهيكلية الأساسية مثل alpha- (α- ) أو beta- (β- ) أو gamma- (γ-) أو delta- (δ-) الأحماض الأمينية ؛ تتعلق الفئات الأخرى بالقطبية ، ومستوى الأس الهيدروجيني ، ونوع مجموعة السلسلة الجانبية (الأليفاتية ، أو الحلقية ، أو العطرية ، أو المحتوية على الهيدروكسيل أو الكبريت ، وما إلى ذلك). في شكل بروتينات ، تشكل بقايا الأحماض الأمينية ثاني أكبر مكون (الماء هو الأكبر) في عضلات الإنسان والأنسجة الأخرى. بالإضافة إلى دورها كبقايا في البروتينات ، تشارك الأحماض الأمينية في عدد من العمليات مثل نقل الناقلات العصبية والتخليق الحيوي. |  |
| حمض أميني: الأحماض الأمينية عبارة عن مركبات عضوية تحتوي على مجموعات وظيفية أمينية (–NH 2 ) وكربوكسيل (–COOH) ، جنبًا إلى جنب مع سلسلة جانبية (مجموعة R) خاصة بكل حمض أميني. العناصر الرئيسية للحمض الأميني هي الكربون (C) والهيدروجين (H) والأكسجين (O) والنيتروجين (N) ، على الرغم من وجود عناصر أخرى في السلاسل الجانبية لبعض الأحماض الأمينية. يُعرف حوالي 500 من الأحماض الأمينية التي تحدث بشكل طبيعي اعتبارًا من عام 1983 (على الرغم من ظهور 20 فقط في الشفرة الوراثية) ويمكن تصنيفها بعدة طرق. يمكن تصنيفها وفقًا لمواقع المجموعات الوظيفية الهيكلية الأساسية مثل alpha- (α- ) أو beta- (β- ) أو gamma- (γ-) أو delta- (δ-) الأحماض الأمينية ؛ تتعلق الفئات الأخرى بالقطبية ، ومستوى الأس الهيدروجيني ، ونوع مجموعة السلسلة الجانبية (الأليفاتية ، أو الحلقية ، أو العطرية ، أو المحتوية على الهيدروكسيل أو الكبريت ، وما إلى ذلك). في شكل بروتينات ، تشكل بقايا الأحماض الأمينية ثاني أكبر مكون (الماء هو الأكبر) في عضلات الإنسان والأنسجة الأخرى. بالإضافة إلى دورها كبقايا في البروتينات ، تشارك الأحماض الأمينية في عدد من العمليات مثل نقل الناقلات العصبية والتخليق الحيوي. |  |
| متفرعة من الأحماض الأمينية سلسلة: الحمض الأميني ذو السلسلة المتفرعة ( BCAA ) هو حمض أميني له سلسلة جانبية أليفاتية مع فرع. من بين الأحماض الأمينية البروتينية ، هناك ثلاثة أحماض أمينية متفرعة السلسلة: ليسين ، آيسولوسين ، وفالين. تشتمل BCAAs غير البروتينية على حمض 2-aminoisobutyric. | 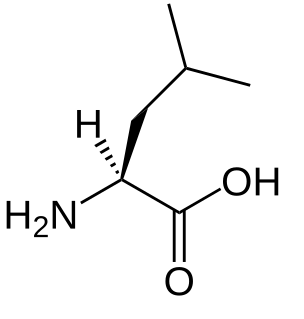 |
| الأحماض الأمينية الأساسية: الحمض الأميني الأساسي ، أو الأحماض الأمينية التي لا غنى عنها ، هو حمض أميني لا يمكن للكائن تصنيعه من الصفر بسرعة كافية لتلبية احتياجاته ، وبالتالي يجب أن يأتي من النظام الغذائي. من بين الأحماض الأمينية الـ 21 الشائعة في جميع أشكال الحياة ، فإن الأحماض الأمينية التسعة التي لا يستطيع البشر تصنيعها هي فينيل ألانين ، فالين ، ثريونين ، تريبتوفان ، ميثيونين ، ليوسين ، إيزولوسين ، ليسين ، وهستيدين. | |
| حمض أميني: الأحماض الأمينية عبارة عن مركبات عضوية تحتوي على مجموعات وظيفية أمينية (–NH 2 ) وكربوكسيل (–COOH) ، جنبًا إلى جنب مع سلسلة جانبية (مجموعة R) خاصة بكل حمض أميني. العناصر الرئيسية للحمض الأميني هي الكربون (C) والهيدروجين (H) والأكسجين (O) والنيتروجين (N) ، على الرغم من وجود عناصر أخرى في السلاسل الجانبية لبعض الأحماض الأمينية. يُعرف حوالي 500 من الأحماض الأمينية التي تحدث بشكل طبيعي اعتبارًا من عام 1983 (على الرغم من ظهور 20 فقط في الشفرة الوراثية) ويمكن تصنيفها بعدة طرق. يمكن تصنيفها وفقًا لمواقع المجموعات الوظيفية الهيكلية الأساسية مثل alpha- (α- ) أو beta- (β- ) أو gamma- (γ-) أو delta- (δ-) الأحماض الأمينية ؛ تتعلق الفئات الأخرى بالقطبية ، ومستوى الأس الهيدروجيني ، ونوع مجموعة السلسلة الجانبية (الأليفاتية ، أو الحلقية ، أو العطرية ، أو المحتوية على الهيدروكسيل أو الكبريت ، وما إلى ذلك). في شكل بروتينات ، تشكل بقايا الأحماض الأمينية ثاني أكبر مكون (الماء هو الأكبر) في عضلات الإنسان والأنسجة الأخرى. بالإضافة إلى دورها كبقايا في البروتينات ، تشارك الأحماض الأمينية في عدد من العمليات مثل نقل الناقلات العصبية والتخليق الحيوي. |  |
| نيتروجين الخميرة: نيتروجين الخميرة أو YAN هو مزيج من النيتروجين الأميني الحر (FAN) والأمونيا (NH 3 ) والأمونيوم (NH 4 + ) المتاح لخميرة النبيذ Saccharomyces cerevisiae لاستخدامه أثناء التخمير. بعيدًا عن السكريات القابلة للتخمير ، الجلوكوز والفركتوز ، يعد النيتروجين أهم العناصر الغذائية اللازمة لإجراء عملية تخمير ناجحة لا تنتهي قبل نقطة الجفاف المقصودة أو تشهد تطور الروائح الكريهة وأعطال النبيذ ذات الصلة. إلى هذا الحد ، غالبًا ما يكمل صانعو النبيذ موارد YAN المتاحة بإضافات النيتروجين مثل فوسفات ثنائي الأمونيوم (DAP). |  |
| نيتروجين الخميرة: نيتروجين الخميرة أو YAN هو مزيج من النيتروجين الأميني الحر (FAN) والأمونيا (NH 3 ) والأمونيوم (NH 4 + ) المتاح لخميرة النبيذ Saccharomyces cerevisiae لاستخدامه أثناء التخمير. بعيدًا عن السكريات القابلة للتخمير ، الجلوكوز والفركتوز ، يعد النيتروجين أهم العناصر الغذائية اللازمة لإجراء عملية تخمير ناجحة لا تنتهي قبل نقطة الجفاف المقصودة أو تشهد تطور الروائح الكريهة وأعطال النبيذ ذات الصلة. إلى هذا الحد ، غالبًا ما يكمل صانعو النبيذ موارد YAN المتاحة بإضافات النيتروجين مثل فوسفات ثنائي الأمونيوم (DAP). |  |
| إنزيم Aminoacyl tRNA synthetase: إنزيم aminoacyl-tRNA synthetase ، والذي يُطلق عليه أيضًا اسم tRNA-ligase ، هو إنزيم يربط الحمض الأميني المناسب بالحمض النووي الريبي المقابل له. يقوم بذلك عن طريق تحفيز الاسترة التبادلية لحمض أميني مشابه أو سلائفه لواحد من جميع tRNAs المتوافقة المتوافقة لتشكيل aminoacyl-tRNA. في البشر ، يتم تصنيع 20 نوعًا مختلفًا من aa-tRNA بواسطة 20 تركيبة مختلفة من aminoacyl-tRNA ، واحدة لكل حمض أميني في الشفرة الوراثية. | 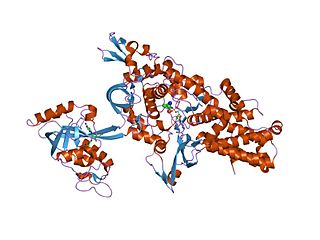 |
| إنزيم Aminoacyl tRNA synthetase: إنزيم aminoacyl-tRNA synthetase ، والذي يُطلق عليه أيضًا اسم tRNA-ligase ، هو إنزيم يربط الحمض الأميني المناسب بالحمض النووي الريبي المقابل له. يقوم بذلك عن طريق تحفيز الاسترة التبادلية لحمض أميني مشابه أو سلائفه لواحد من جميع tRNAs المتوافقة المتوافقة لتشكيل aminoacyl-tRNA. في البشر ، يتم تصنيع 20 نوعًا مختلفًا من aa-tRNA بواسطة 20 تركيبة مختلفة من aminoacyl-tRNA ، واحدة لكل حمض أميني في الشفرة الوراثية. |  |
| الكانولامين: Alkanolamines هي مركبات كيميائية تحتوي على كل من الهيدروكسيل (-OH) والمجموعات الأمينية (-NH 2 و -NHR و -NR 2 ) على العمود الفقري للألكان. مصطلح الكانولامين هو مصطلح فئة واسع يستخدم في بعض الأحيان كتصنيف فرعي. | |
| الكانولامين: Alkanolamines هي مركبات كيميائية تحتوي على كل من الهيدروكسيل (-OH) والمجموعات الأمينية (-NH 2 و -NHR و -NR 2 ) على العمود الفقري للألكان. مصطلح الكانولامين هو مصطلح فئة واسع يستخدم في بعض الأحيان كتصنيف فرعي. | |
| الأنيلين: الأنيلين مركب عضوي بالصيغة C 6 H 5 NH 2 . يتكون الأنيلين من مجموعة فينيل مرتبطة بمجموعة أمينية ، وهو أبسط أمين عطري. إنها مادة كيميائية سلعة مهمة صناعيًا ، فضلاً عن كونها مادة انطلاق متعددة الاستخدامات لتخليق كيميائي جيد. يتم استخدامه الرئيسي في تصنيع سلائف البولي يوريثين والأصباغ والمواد الكيميائية الصناعية الأخرى. مثل معظم الأمينات المتطايرة ، لها رائحة الأسماك الفاسدة. يشتعل بسهولة ، ويحترق بلهب مدخن من خصائص المركبات العطرية. |  |
| السندات الببتيد: الرابطة الببتيدية هي نوع أميد من الرابطة الكيميائية التساهمية التي تربط بين اثنين من الأحماض الأمينية ألفا متتالية من C1 لحمض ألفا أميني واحد و N2 من حمض آخر ، على طول سلسلة الببتيد أو البروتين. |  |
| حمض أمينوكابرويك: حمض أمينوكابرويك هو مشتق وتماثلي للحمض الأميني ليسين ، مما يجعله مثبطًا فعالًا للأنزيمات التي تربط هذه البقايا المعينة. وتشمل هذه الإنزيمات الإنزيمات المحللة للبروتين مثل البلازمين ، وهو الإنزيم المسؤول عن انحلال الفبرين. لهذا السبب فهو فعال في علاج بعض اضطرابات النزيف ، ويباع تحت الاسم التجاري Amicar . حمض أمينوكابرويك هو أيضًا وسيط في بلمرة نايلون 6 ، حيث يتشكل عن طريق التحلل المائي للفتحة الحلقية للكابرولاكتام. أظهر تحديد التركيب البلوري أن حمض 6-aminohexanoic موجود كملح ، على الأقل في الحالة الصلبة. |  |
| إسترات أمينية: الإسترات الأمينية هي فئة من أدوية التخدير الموضعي. تم تسميتهم من أجل رابطة استر. | |
| أمين: في الكيمياء العضوية ، الأمينات ( المملكة المتحدة أيضًا ) عبارة عن مركبات ومجموعات وظيفية تحتوي على ذرة نيتروجين أساسية مع زوج وحيد. الأمينات هي مشتقات رسمية للأمونيا ، حيث يتم استبدال ذرة هيدروجين واحدة أو أكثر بمواد بديلة مثل مجموعة ألكيل أو أريل (يمكن أن يطلق عليها على التوالي ألكيل أمين وأريلامين ؛ قد يتم ربط كلا النوعين من المواد البديلة بذرة نيتروجين واحدة أن تسمى ألكيلريل أمين). الأمينات الهامة تشمل الأحماض الأمينية ، الأمينات الحيوية ، ثلاثي ميثيل أمين ، والأنيلين. انظر التصنيف: الأمينات للحصول على قائمة الأمينات. تسمى المشتقات غير العضوية للأمونيا أيضًا بالأمينات ، مثل أحادي الكلورامين (NClH 2 ). | |
| أمينوغليكوزيد: الأمينوغليكوزيد هو فئة طبية وبكتريولوجية من الأدوية المضادة للبكتيريا سالبة الجرام التقليدية التي تمنع تخليق البروتين وتحتوي كجزء من الجزيء على جليكوسيد معدل أمينيًا (سكر). يمكن أن يشير المصطلح أيضًا بشكل أكثر عمومية إلى أي جزيء عضوي يحتوي على تركيبات السكر الأمينية. تُظهر المضادات الحيوية أمينوغليكوزيد نشاطًا مبيدًا للجراثيم ضد البكتيريا الهوائية سالبة الجرام وبعض العصيات اللاهوائية حيث لم تظهر المقاومة بعد ولكن بشكل عام ليس ضد البكتيريا موجبة الجرام واللاهوائية سالبة الجرام. | 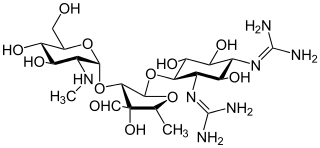 |
| أمين: في الكيمياء العضوية ، الأمينات ( المملكة المتحدة أيضًا ) عبارة عن مركبات ومجموعات وظيفية تحتوي على ذرة نيتروجين أساسية مع زوج وحيد. الأمينات هي مشتقات رسمية للأمونيا ، حيث يتم استبدال ذرة هيدروجين واحدة أو أكثر بمواد بديلة مثل مجموعة ألكيل أو أريل (يمكن أن يطلق عليها على التوالي ألكيل أمين وأريلامين ؛ قد يتم ربط كلا النوعين من المواد البديلة بذرة نيتروجين واحدة أن تسمى ألكيلريل أمين). الأمينات الهامة تشمل الأحماض الأمينية ، الأمينات الحيوية ، ثلاثي ميثيل أمين ، والأنيلين. انظر التصنيف: الأمينات للحصول على قائمة الأمينات. تسمى المشتقات غير العضوية للأمونيا أيضًا بالأمينات ، مثل أحادي الكلورامين (NClH 2 ). | |
| 2-حمض أمينويوبيريك 2-Aminoisobutyric acid (المعروف أيضًا باسم حمض α-aminoisobutyric أو AIB أو α-methylalanine أو 2-methylalanine ) هو حمض أميني غير بروتيني المنشأ مع الصيغة الهيكلية H 2 NC (CH 3 ) 2 -COOH. إنه نادر في الطبيعة ، حيث يوجد فقط في النيازك ، وبعض المضادات الحيوية من أصل فطري ، مثل الألاميثيسين وبعض المضادات الحيوية. | 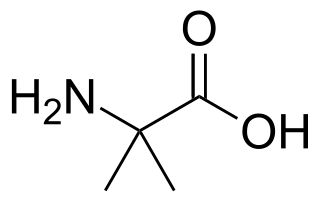 |
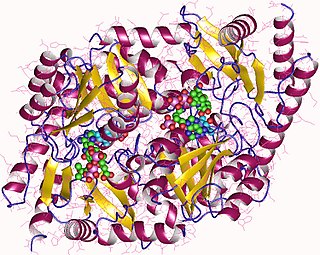
| سينثاس حمض أمينوليفولينك: سينثاز حمض أمينوليفولينيك ( ALA synthase ، ALAS ، أو delta-aminolevulinic acid synthase ) هو إنزيم (EC 2.3.1.37 ) يحفز تركيب حمض δ-aminolevulinic (ALA) ، وهو أول سلائف شائعة في التخليق الحيوي لجميع مركبات رباعي البيرول. والكوبالامينات والكلوروفيل. رد الفعل على النحو التالي:
|  |
| أمين: في الكيمياء العضوية ، الأمينات ( المملكة المتحدة أيضًا ) عبارة عن مركبات ومجموعات وظيفية تحتوي على ذرة نيتروجين أساسية مع زوج وحيد. الأمينات هي مشتقات رسمية للأمونيا ، حيث يتم استبدال ذرة هيدروجين واحدة أو أكثر بمواد بديلة مثل مجموعة ألكيل أو أريل (يمكن أن يطلق عليها على التوالي ألكيل أمين وأريلامين ؛ قد يتم ربط كلا النوعين من المواد البديلة بذرة نيتروجين واحدة أن تسمى ألكيلريل أمين). الأمينات الهامة تشمل الأحماض الأمينية ، الأمينات الحيوية ، ثلاثي ميثيل أمين ، والأنيلين. انظر التصنيف: الأمينات للحصول على قائمة الأمينات. تسمى المشتقات غير العضوية للأمونيا أيضًا بالأمينات ، مثل أحادي الكلورامين (NClH 2 ). | |
| الراديكالية الأمينية: الراديكالية الأمينية ، • | |
| السكر الأميني: في الكيمياء العضوية ، السكر الأميني هو جزيء سكر حيث تم استبدال مجموعة الهيدروكسيل بمجموعة أمين. أكثر من 60 سكريات أمينية معروفة ، وأكثرها وفرة هو N -Acetyl- d -glucosamine ، وهو المكون الرئيسي للكيتين. | 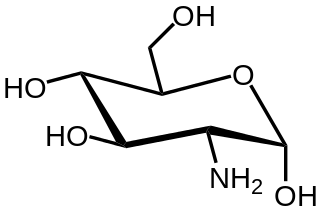 |
| السكر الأميني: في الكيمياء العضوية ، السكر الأميني هو جزيء سكر حيث تم استبدال مجموعة الهيدروكسيل بمجموعة أمين. أكثر من 60 سكريات أمينية معروفة ، وأكثرها وفرة هو N -Acetyl- d -glucosamine ، وهو المكون الرئيسي للكيتين. |  |
| السكر الأميني: في الكيمياء العضوية ، السكر الأميني هو جزيء سكر حيث تم استبدال مجموعة الهيدروكسيل بمجموعة أمين. أكثر من 60 سكريات أمينية معروفة ، وأكثرها وفرة هو N -Acetyl- d -glucosamine ، وهو المكون الرئيسي للكيتين. |  |
| الأسبارتام: الأسبارتام هو مُحلي صناعي خالٍ من السكريات أحلى 200 مرة من السكروز ، ويستخدم عادة كبديل للسكر في الأطعمة والمشروبات. وهو إستر ميثيل لحمض الأسبارتيك / ثنائي ببتيد فينيل ألانين مع الأسماء التجارية NutraSweet و Equal و Canderel . تم تصنيع الأسبارتام لأول مرة في عام 1965 وتمت الموافقة عليه للاستخدام في المنتجات الغذائية من قبل إدارة الغذاء والدواء الأمريكية (FDA) في عام 1981. |  |
| N- المحطة: إن الطرف N (المعروف أيضًا باسم الطرف الأميني ، NH 2 -terminus ، N-terminal أو نهاية amine-terminus ) هو بداية بروتين أو عديد ببتيد يشير إلى مجموعة الأمين الحرة (-NH 2 ) الموجودة في النهاية من عديد ببتيد. داخل الببتيد ، ترتبط مجموعة الأمين بمجموعة كربوكسيلية أخرى في بروتين لجعلها سلسلة ، ولكن نظرًا لأن نهاية الحمض الأميني للبروتين متصل فقط بنهاية الكربوكسيد ، فإن مجموعة الأمين الحرة المتبقية تسمى N- نهاية. وفقًا للاتفاقية ، تتم كتابة متواليات الببتيد N-terminus إلى C-terminus ، من اليسار إلى اليمين (في أنظمة كتابة LTR). يربط هذا اتجاه الترجمة باتجاه النص (لأنه عندما يُترجم بروتين من RNA الرسول ، يتم إنشاؤه من N-terminus إلى C-terminus - تُضاف الأحماض الأمينية إلى نهاية الكربوكسيل). | |
| N- المحطة: إن الطرف N (المعروف أيضًا باسم الطرف الأميني ، NH 2 -terminus ، N-terminal أو نهاية amine-terminus ) هو بداية بروتين أو عديد ببتيد يشير إلى مجموعة الأمين الحرة (-NH 2 ) الموجودة في النهاية من عديد ببتيد. داخل الببتيد ، ترتبط مجموعة الأمين بمجموعة كربوكسيلية أخرى في بروتين لجعلها سلسلة ، ولكن نظرًا لأن نهاية الحمض الأميني للبروتين متصل فقط بنهاية الكربوكسيد ، فإن مجموعة الأمين الحرة المتبقية تسمى N- نهاية. وفقًا للاتفاقية ، تتم كتابة متواليات الببتيد N-terminus إلى C-terminus ، من اليسار إلى اليمين (في أنظمة كتابة LTR). يربط هذا اتجاه الترجمة باتجاه النص (لأنه عندما يُترجم بروتين من RNA الرسول ، يتم إنشاؤه من N-terminus إلى C-terminus - تُضاف الأحماض الأمينية إلى نهاية الكربوكسيل). | |
| امينال: aminal أو aminoacetal عبارة عن مجموعة وظيفية أو نوع من المركبات العضوية التي تحتوي على مجموعتين أمينيتين متصلتين بذرة الكربون نفسها: -C (NR 2 ) (NR 2 ) -. (كما هو معتاد في الكيمياء العضوية ، يمكن أن تمثل R هيدروجين أو مجموعة ألكيل). |  |
| أمينو أسيتالدهيد: Aminoacetaldehyde هو مركب عضوي بالصيغة OHCCH 2 NH 2 . في ظل الظروف المعملية المعتادة ، يكون غير مستقر ، ويميل بدلاً من ذلك إلى الخضوع للتكثيف الذاتي. Aminoacetaldehyde diethylacetal هو بديل مستقر. |  |
| أمينو أسيتالدهيد ثنائي إثيل أسيتال: Aminoacetaldehyde diethylacetal هو مركب عضوي له الصيغة (EtO) 2 CHCH 2 NH 2 . سائل عديم اللون ، يستخدم كبديل للأمينو أسيتالدهيد. | 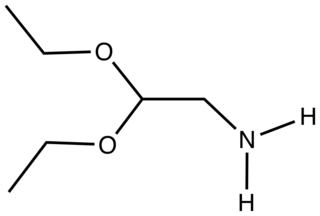 |
| جليكاين: الجليسين (الرمز Gly أو G ؛) هو حمض أميني يحتوي على ذرة هيدروجين واحدة كسلسلة جانبية. إنه أبسط حمض أميني ثابت (حمض الكرباميك غير مستقر) ، مع الصيغة الكيميائية NH 2 - CH 2 ‐COOH. الجلايسين هو أحد الأحماض الأمينية البروتينية. يتم ترميزه بواسطة جميع الكودونات التي تبدأ بـ GG (GGU ، GGC ، GGA ، GGG). يعتبر الجلايسين جزءًا لا يتجزأ من تكوين حلزونات ألفا في بنية البروتين الثانوية نظرًا لشكله المضغوط. للسبب نفسه ، فهو أكثر الأحماض الأمينية وفرة في الكولاجين الثلاثي الحلزونات. الجليسين هو أيضًا ناقل عصبي مثبط - يمكن أن يتسبب التداخل في إطلاقه داخل الحبل الشوكي (كما يحدث أثناء عدوى المطثية الكزازية ) في حدوث شلل تشنجي بسبب تقلص العضلات غير المقيد. |  |
| أمينو أسيتون: Aminoacetone هو مركب عضوي بالصيغة CH 3 C (O) CH 2 NH 2 . على الرغم من ثباته في الشكل الغازي ، إلا أنه بمجرد تكثيفه يتفاعل مع نفسه. يشكل المشتق البروتوني أملاحًا مستقرة ، مثل aminoacetone hydrochloride ([CH 3 C (O) CH 2 NH 3 ] Cl)). يعتبر semicarbazone للهيدروكلوريد مادة أخرى مستقرة على مقاعد البدلاء. Aminoacetone هو مستقلب متورط في التخليق الحيوي للميثيل جليوكسال. |  |
| أمينو أسيتونيتريل: Aminoacetonitrile هو مركب عضوي مع الصيغة NCCH 2 NH 2 . المركب سائل عديم اللون. إنه غير مستقر في درجة حرارة الغرفة ، بسبب عدم توافق النوكليوفيل الأمين والنتريل الكهربائي. لهذا السبب يتم مواجهتها عادةً على شكل أملاح كلوريد وثنائي كبريتات مشتق الأمونيوم ، أي [NCCH 2 NH 3 ] + Cl - و [NCCH 2 NH 3 ] + HSO 4 - . | |
| حمض أميني: الأحماض الأمينية عبارة عن مركبات عضوية تحتوي على مجموعات وظيفية أمينية (–NH 2 ) وكربوكسيل (–COOH) ، جنبًا إلى جنب مع سلسلة جانبية (مجموعة R) خاصة بكل حمض أميني. العناصر الرئيسية للحمض الأميني هي الكربون (C) والهيدروجين (H) والأكسجين (O) والنيتروجين (N) ، على الرغم من وجود عناصر أخرى في السلاسل الجانبية لبعض الأحماض الأمينية. يُعرف حوالي 500 من الأحماض الأمينية التي تحدث بشكل طبيعي اعتبارًا من عام 1983 (على الرغم من ظهور 20 فقط في الشفرة الوراثية) ويمكن تصنيفها بعدة طرق. يمكن تصنيفها وفقًا لمواقع المجموعات الوظيفية الهيكلية الأساسية مثل alpha- (α- ) أو beta- (β- ) أو gamma- (γ-) أو delta- (δ-) الأحماض الأمينية ؛ تتعلق الفئات الأخرى بالقطبية ، ومستوى الأس الهيدروجيني ، ونوع مجموعة السلسلة الجانبية (الأليفاتية ، أو الحلقية ، أو العطرية ، أو المحتوية على الهيدروكسيل أو الكبريت ، وما إلى ذلك). في شكل بروتينات ، تشكل بقايا الأحماض الأمينية ثاني أكبر مكون (الماء هو الأكبر) في عضلات الإنسان والأنسجة الأخرى. بالإضافة إلى دورها كبقايا في البروتينات ، تشارك الأحماض الأمينية في عدد من العمليات مثل نقل الناقلات العصبية والتخليق الحيوي. |  |
| حمض أميني: الأحماض الأمينية عبارة عن مركبات عضوية تحتوي على مجموعات وظيفية أمينية (–NH 2 ) وكربوكسيل (–COOH) ، جنبًا إلى جنب مع سلسلة جانبية (مجموعة R) خاصة بكل حمض أميني. العناصر الرئيسية للحمض الأميني هي الكربون (C) والهيدروجين (H) والأكسجين (O) والنيتروجين (N) ، على الرغم من وجود عناصر أخرى في السلاسل الجانبية لبعض الأحماض الأمينية. يُعرف حوالي 500 من الأحماض الأمينية التي تحدث بشكل طبيعي اعتبارًا من عام 1983 (على الرغم من ظهور 20 فقط في الشفرة الوراثية) ويمكن تصنيفها بعدة طرق. يمكن تصنيفها وفقًا لمواقع المجموعات الوظيفية الهيكلية الأساسية مثل alpha- (α- ) أو beta- (β- ) أو gamma- (γ-) أو delta- (δ-) الأحماض الأمينية ؛ تتعلق الفئات الأخرى بالقطبية ، ومستوى الأس الهيدروجيني ، ونوع مجموعة السلسلة الجانبية (الأليفاتية ، أو الحلقية ، أو العطرية ، أو المحتوية على الهيدروكسيل أو الكبريت ، وما إلى ذلك). في شكل بروتينات ، تشكل بقايا الأحماض الأمينية ثاني أكبر مكون (الماء هو الأكبر) في عضلات الإنسان والأنسجة الأخرى. بالإضافة إلى دورها كبقايا في البروتينات ، تشارك الأحماض الأمينية في عدد من العمليات مثل نقل الناقلات العصبية والتخليق الحيوي. |  |
| بيلة أمينية: تحدث البيلة الأمينية عندما يحتوي البول على كميات عالية بشكل غير طبيعي من الأحماض الأمينية. في الكلى السليمة ، ترشح الكبيبات جميع الأحماض الأمينية من الدم ، ثم تعيد الأنابيب الكلوية امتصاص أكثر من 95٪ من الأحماض الأمينية المفلترة في الدم. |  |
| بيلة أمينية: تحدث البيلة الأمينية عندما يحتوي البول على كميات عالية بشكل غير طبيعي من الأحماض الأمينية. في الكلى السليمة ، ترشح الكبيبات جميع الأحماض الأمينية من الدم ، ثم تعيد الأنابيب الكلوية امتصاص أكثر من 95٪ من الأحماض الأمينية المفلترة في الدم. |  |
| أمينوكريدين: قد يشير Aminoacridine إلى أي من المركبات الكيميائية العديدة:
| |
| أمينوكريدين: قد يشير Aminoacridine إلى أي من المركبات الكيميائية العديدة:
| |
| حمض أميني: الأحماض الأمينية عبارة عن مركبات عضوية تحتوي على مجموعات وظيفية أمينية (–NH 2 ) وكربوكسيل (–COOH) ، جنبًا إلى جنب مع سلسلة جانبية (مجموعة R) خاصة بكل حمض أميني. العناصر الرئيسية للحمض الأميني هي الكربون (C) والهيدروجين (H) والأكسجين (O) والنيتروجين (N) ، على الرغم من وجود عناصر أخرى في السلاسل الجانبية لبعض الأحماض الأمينية. يُعرف حوالي 500 من الأحماض الأمينية التي تحدث بشكل طبيعي اعتبارًا من عام 1983 (على الرغم من ظهور 20 فقط في الشفرة الوراثية) ويمكن تصنيفها بعدة طرق. يمكن تصنيفها وفقًا لمواقع المجموعات الوظيفية الهيكلية الأساسية مثل alpha- (α- ) أو beta- (β- ) أو gamma- (γ-) أو delta- (δ-) الأحماض الأمينية ؛ تتعلق الفئات الأخرى بالقطبية ، ومستوى الأس الهيدروجيني ، ونوع مجموعة السلسلة الجانبية (الأليفاتية ، أو الحلقية ، أو العطرية ، أو المحتوية على الهيدروكسيل أو الكبريت ، وما إلى ذلك). في شكل بروتينات ، تشكل بقايا الأحماض الأمينية ثاني أكبر مكون (الماء هو الأكبر) في عضلات الإنسان والأنسجة الأخرى. بالإضافة إلى دورها كبقايا في البروتينات ، تشارك الأحماض الأمينية في عدد من العمليات مثل نقل الناقلات العصبية والتخليق الحيوي. |  |
| X- له ثنائي ببتيداز: Xaa-His dipeptidase هو إنزيم. هذا الإنزيم يحفز التفاعل الكيميائي التالي
| |
| كارنوزين الدم: كارنوزين الدم ، هو اضطراب استقلابي وراثي متنحي نادر ناجم عن نقص في الكارنوزيناز ، وهو ثنائي ببتيداز. |  |
| إكس أرج ديبيبتيداز: Xaa-Arg dipeptidase هو إنزيم. هذا الإنزيم يحفز التفاعل الكيميائي التالي
| |
| X-methyl-His dipeptidase: Xaa-methyl-His dipeptidase هو إنزيم. هذا الإنزيم يحفز التفاعل الكيميائي التالي
| |
| X-methyl-His dipeptidase: Xaa-methyl-His dipeptidase هو إنزيم. هذا الإنزيم يحفز التفاعل الكيميائي التالي
| |
| Aminoacyl-tRNA: Aminoacyl-tRNA هو الحمض الريبي النووي النقال الذي يرتبط به حمض أميني مشحون كيميائيًا (مشحون). تقوم aa-tRNA ، جنبًا إلى جنب مع عوامل الاستطالة الخاصة ، بتسليم الحمض الأميني إلى الريبوسوم لإدماجه في سلسلة polypeptide التي يتم إنتاجها أثناء الترجمة. |  |
| Aminoacyl-tRNA هيدرولاز: في علم الإنزيمات ، إنزيم aminoacyl -tRNA hydrolase (EC 3.1.1.29 ) هو إنزيم يحفز التفاعل الكيميائي
| |
| Aminoacyl-tRNA هيدرولاز: في علم الإنزيمات ، إنزيم aminoacyl -tRNA hydrolase (EC 3.1.1.29 ) هو إنزيم يحفز التفاعل الكيميائي
| |
| إنزيم Aminoacyl tRNA synthetase: إنزيم aminoacyl-tRNA synthetase ، والذي يُطلق عليه أيضًا اسم tRNA-ligase ، هو إنزيم يربط الحمض الأميني المناسب بالحمض النووي الريبي المقابل له. يقوم بذلك عن طريق تحفيز الاسترة التبادلية لحمض أميني مشابه أو سلائفه لواحد من جميع tRNAs المتوافقة المتوافقة لتشكيل aminoacyl-tRNA. في البشر ، يتم تصنيع 20 نوعًا مختلفًا من aa-tRNA بواسطة 20 تركيبة مختلفة من aminoacyl-tRNA ، واحدة لكل حمض أميني في الشفرة الوراثية. |  |
| إنزيم Aminoacyl tRNA synthetase: إنزيم aminoacyl-tRNA synthetase ، والذي يُطلق عليه أيضًا اسم tRNA-ligase ، هو إنزيم يربط الحمض الأميني المناسب بالحمض النووي الريبي المقابل له. يقوم بذلك عن طريق تحفيز الاسترة التبادلية لحمض أميني مشابه أو سلائفه لواحد من جميع tRNAs المتوافقة المتوافقة لتشكيل aminoacyl-tRNA. في البشر ، يتم تصنيع 20 نوعًا مختلفًا من aa-tRNA بواسطة 20 تركيبة مختلفة من aminoacyl-tRNA ، واحدة لكل حمض أميني في الشفرة الوراثية. |  |
| الريبوسوم: الريبوسومات هي آلات جزيئية كبيرة ، توجد داخل جميع الخلايا الحية ، تقوم بتخليق البروتين البيولوجي. تربط الريبوسومات الأحماض الأمينية معًا بالترتيب المحدد بواسطة أكواد جزيئات الرنا المرسال (mRNA) لتشكيل سلاسل متعددة الببتيد. تتكون الريبوسومات من مكونين رئيسيين: الوحدات الفرعية الريبوسومية الصغيرة والكبيرة. تتكون كل وحدة فرعية من جزيء واحد أو أكثر من جزيئات RNA الريباسي والعديد من بروتينات الريبوسوم. تُعرف الريبوسومات والجزيئات المرتبطة بها أيضًا باسم الجهاز الانتقالي . |  |
| Aminoacyl-tRNA: Aminoacyl-tRNA هو الحمض الريبي النووي النقال الذي يرتبط به حمض أميني مشحون كيميائيًا (مشحون). تقوم aa-tRNA ، جنبًا إلى جنب مع عوامل الاستطالة الخاصة ، بتسليم الحمض الأميني إلى الريبوسوم لإدماجه في سلسلة polypeptide التي يتم إنتاجها أثناء الترجمة. |  |
| إنزيم Aminoacyl tRNA synthetase: إنزيم aminoacyl-tRNA synthetase ، والذي يُطلق عليه أيضًا اسم tRNA-ligase ، هو إنزيم يربط الحمض الأميني المناسب بالحمض النووي الريبي المقابل له. يقوم بذلك عن طريق تحفيز الاسترة التبادلية لحمض أميني مشابه أو سلائفه لواحد من جميع tRNAs المتوافقة المتوافقة لتشكيل aminoacyl-tRNA. في البشر ، يتم تصنيع 20 نوعًا مختلفًا من aa-tRNA بواسطة 20 تركيبة مختلفة من aminoacyl-tRNA ، واحدة لكل حمض أميني في الشفرة الوراثية. |  |
| إنزيم Aminoacyl tRNA synthetase: إنزيم aminoacyl-tRNA synthetase ، والذي يُطلق عليه أيضًا اسم tRNA-ligase ، هو إنزيم يربط الحمض الأميني المناسب بالحمض النووي الريبي المقابل له. يقوم بذلك عن طريق تحفيز الاسترة التبادلية لحمض أميني مشابه أو سلائفه لواحد من جميع tRNAs المتوافقة المتوافقة لتشكيل aminoacyl-tRNA. في البشر ، يتم تصنيع 20 نوعًا مختلفًا من aa-tRNA بواسطة 20 تركيبة مختلفة من aminoacyl-tRNA ، واحدة لكل حمض أميني في الشفرة الوراثية. |  |
| إنزيم Aminoacyl tRNA synthetase: إنزيم aminoacyl-tRNA synthetase ، والذي يُطلق عليه أيضًا اسم tRNA-ligase ، هو إنزيم يربط الحمض الأميني المناسب بالحمض النووي الريبي المقابل له. يقوم بذلك عن طريق تحفيز الاسترة التبادلية لحمض أميني مشابه أو سلائفه لواحد من جميع tRNAs المتوافقة المتوافقة لتشكيل aminoacyl-tRNA. في البشر ، يتم تصنيع 20 نوعًا مختلفًا من aa-tRNA بواسطة 20 تركيبة مختلفة من aminoacyl-tRNA ، واحدة لكل حمض أميني في الشفرة الوراثية. |  |
| إنزيم Aminoacyl tRNA synthetase: إنزيم aminoacyl-tRNA synthetase ، والذي يُطلق عليه أيضًا اسم tRNA-ligase ، هو إنزيم يربط الحمض الأميني المناسب بالحمض النووي الريبي المقابل له. يقوم بذلك عن طريق تحفيز الاسترة التبادلية لحمض أميني مشابه أو سلائفه لواحد من جميع tRNAs المتوافقة المتوافقة لتشكيل aminoacyl-tRNA. في البشر ، يتم تصنيع 20 نوعًا مختلفًا من aa-tRNA بواسطة 20 تركيبة مختلفة من aminoacyl-tRNA ، واحدة لكل حمض أميني في الشفرة الوراثية. |  |
| إنزيم Aminoacyl tRNA synthetase: إنزيم aminoacyl-tRNA synthetase ، والذي يُطلق عليه أيضًا اسم tRNA-ligase ، هو إنزيم يربط الحمض الأميني المناسب بالحمض النووي الريبي المقابل له. يقوم بذلك عن طريق تحفيز الاسترة التبادلية لحمض أميني مشابه أو سلائفه لواحد من جميع tRNAs المتوافقة المتوافقة لتشكيل aminoacyl-tRNA. في البشر ، يتم تصنيع 20 نوعًا مختلفًا من aa-tRNA بواسطة 20 تركيبة مختلفة من aminoacyl-tRNA ، واحدة لكل حمض أميني في الشفرة الوراثية. |  |
| المواد التركيبية Aminoacyl tRNA ، الفئة الأولى: تحفز المواد التركيبية aminoacyl-tRNA ارتباط الحمض الأميني بجزيء الحمض النووي الريبي المرتبط بنقله المشابه في تفاعل عالي التحديد من خطوتين. تختلف هذه البروتينات على نطاق واسع في الحجم والحالة القلة العددية ، ولها تجانس تسلسل محدود. تنقسم تركيبات 20 aminoacyl-tRNA إلى فئتين ، الأول والثاني. تحتوي تركيبات الصنف الأول من aminoacyl-tRNA على مجال تحفيزي خاص بطيات Rossmann وهو في الغالب أحادي. تشترك المواد التركيبية aminoacyl-tRNA من الفئة الثانية في طية صفائح بيتا متوازية محاطة بحلزونات ألفا ، وتكون في الغالب قاتمة أو متعددة ، وتحتوي على ثلاث مناطق محفوظة على الأقل. ومع ذلك ، فإن ارتباط الحمض الريبي النووي النقال (tRNA) يتضمن بنية ألفا حلزونية يتم حفظها بين تركيبات الصنف الأول والفئة الثانية. في التفاعلات المحفزة بواسطة تركيبات aminoacyl-tRNA من الفئة الأولى ، تقترن مجموعة aminoacyl بـ 2'-hydroxyl من tRNA ، بينما ، في تفاعلات الفئة II ، يُفضل موقع 3'-hydroxyl. المواد التركيبية الخاصة بالأرجينين ، والسيستين ، وحمض الجلوتاميك ، والجلوتامين ، والإيزولوسين ، والليوسين ، والميثيونين ، والتيروزين ، والتربتوفان ، والفالين تنتمي إلى الصنف الأول التركيبي ؛ وتنقسم هذه التركيبات أيضًا إلى ثلاث فئات فرعية ، أ ، ب ، ج وفقًا لتماثل التسلسل. المواد التركيبية الخاصة بالألانين ، الأسباراجين ، حمض الأسبارتيك ، الجلايسين ، الهيستيدين ، اللايسين ، الفنيل ألانين ، البرولين ، السيرين ، والثريونين تنتمي إلى الصنف الثاني. | |
| تركيبة Aminoacyl tRNA ، الفئة الثانية تركيبة Aminoacyl-tRNA ، الفئة الثانية هي عائلة من البروتينات. تعمل هذه البروتينات على تحفيز ارتباط الحمض الأميني بجزيء RNA الناقل له في تفاعل عالي التحديد من خطوتين. تختلف هذه البروتينات على نطاق واسع في الحجم والحالة القلية ، ولها تسلسل محدود. |
بحث هذه المدونة الإلكترونية
الأربعاء، 9 يونيو 2021
Aspartame, Amino (app), Amino (app)
الاشتراك في:
تعليقات الرسالة (Atom)
-
علي بن محزيار الأهواز: كان علي بن محزيار الأحوازي عالمًا قضائيًا شيعيًا مبكرًا وبارزًا وراويًا وعالمًا. محزيار عالم من القرن التاسع و...
-
مسجد علي بيتشن: مسجد علي بيتشين أو مسجد Zawj Euyun هو مسجد تاريخي في الجزائر العاصمة ، الجزائر. أمر علي بيتشن ببناء المسجد في عام ...
-
علي فاركا توري: كان علي إبراهيم " علي فركة " توري مغنيًا ماليًا وعازفًا متعدد الآلات ، وأحد أشهر الموسيقيين في القارة الأف...

ليست هناك تعليقات:
إرسال تعليق